Реакции переноса электронов
Элементарные стадии с участием комплексов металлов
Реакции металлокомплексов можно разделить на три группы:
а) реакции переноса электрона;
б) реакции замещения лигандов;
в) реакции координированных лигандов.
Реакции переноса электронов
Два механизма реализуются в реакциях переноса электронов – внешнесферный механизм (без изменений в координационных сферах донора и акцептора) и мостиковый (внутрисферный) механизм, приводящий к изменениям в координационной сфере металла.
Рассмотрим внешнесферный механизм на примере октаэдрических комплексов переходных металлов. В случае симметричных реакций (DG0 = 0)

константы скорости меняются в очень широком интервале значений – от 10–12 до 105 л·моль–1·сек–1, в зависимости от электронной конфигурации иона и степени ее перестройки в ходе процесса. В этих реакциях очень наглядно проявляется принцип наименьшего движения – наименьшего изменения валентной оболочки участников реакции.
В реакции переноса электрона (1) (Со* – изотоп атома Со)
 (1)
(1)
 (симметричная реакция), Co2+ (d7) переходит в Co3+ (d6). Электронная конфигурация (валентная оболочка) в ходе этого переноса не меняется
(симметричная реакция), Co2+ (d7) переходит в Co3+ (d6). Электронная конфигурация (валентная оболочка) в ходе этого переноса не меняется

6 электронов на трижды вырожденном связывающем уровне остаются без изменения ( 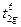 ), а с разрыхляющего eg уровня снимается один электрон. Константа скорости второго порядка для реакции (1) k1 = 1.1 л×моль–1×сек–1. Поскольку Phen (фенантролин) относится к сильным лигандам, максимальное число из 7 d-электронов спарено (спин-спаренное состояние). В случае слабого лиганда NH3 ситуация кардинально меняется. Co(NH3)n2+ (n = 4, 5, 6) находится в спин-неспаренном (высокоспиновом) состоянии
), а с разрыхляющего eg уровня снимается один электрон. Константа скорости второго порядка для реакции (1) k1 = 1.1 л×моль–1×сек–1. Поскольку Phen (фенантролин) относится к сильным лигандам, максимальное число из 7 d-электронов спарено (спин-спаренное состояние). В случае слабого лиганда NH3 ситуация кардинально меняется. Co(NH3)n2+ (n = 4, 5, 6) находится в спин-неспаренном (высокоспиновом) состоянии  .
.

Более прочный комплекс Co(NH3)63+ (прочнее Co(NH3)62+ ~ в 1030 раз) находится в спин-спаренном состоянии 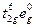 , как и комплекс с Phen. Поэтому в процессе переноса электрона
, как и комплекс с Phen. Поэтому в процессе переноса электрона  должна сильно перестроиться валентная оболочка и в результате k = 10–9 л×моль–1×сек–1. Степень превращения Со2+ в Со3+, равная 50%, достигается в случае лиганда Phen за 1 секунду, а в случае NH3 ~ за 30 лет. Очевидно, что стадию с такой скоростью (формально элементарную) можно исключить из набора элементарных стадий при анализе механизмов реакции.
должна сильно перестроиться валентная оболочка и в результате k = 10–9 л×моль–1×сек–1. Степень превращения Со2+ в Со3+, равная 50%, достигается в случае лиганда Phen за 1 секунду, а в случае NH3 ~ за 30 лет. Очевидно, что стадию с такой скоростью (формально элементарную) можно исключить из набора элементарных стадий при анализе механизмов реакции.
Величина DG¹ для реакции переноса электронов при образовании комплекса столкновения согласно теории Маркуса включает два компонента  и
и 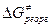
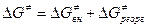 (2)
(2)
Первый член – энергия реорганизации связей M-L внутри комплекса (длина и прочность связи при изменении валентного состояния). Величина 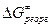 включает энергию перестройки внешней сольватной оболочки в процессе изменения координат M-L и заряда комплекса. Чем меньше изменение электронного окружения и меньше изменение длины M-L, тем ниже
включает энергию перестройки внешней сольватной оболочки в процессе изменения координат M-L и заряда комплекса. Чем меньше изменение электронного окружения и меньше изменение длины M-L, тем ниже  , чем больше по размерам лиганды, тем меньше
, чем больше по размерам лиганды, тем меньше 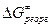 и, в результате, выше скорость переноса электронов. Величину
и, в результате, выше скорость переноса электронов. Величину  для общего случая можно рассчитать по уравнению Маркуса
для общего случая можно рассчитать по уравнению Маркуса
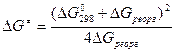 , (3)
, (3)
где 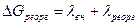 . При
. При  = 0
= 0  .
.
В случае внутрисферного механизма процесс переноса электрона облегчается, поскольку один из лигандов первого комплекса образует мостиковый комплекс со вторым комплексом, вытесняя из него один из лигандов

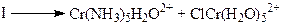
Константы скорости такого процесса на 8 порядков выше константы для восстановления Cr(NH3)63+. В таких реакциях восстанавливающий агент должен быть лабильным комплексом, а лиганд в окислителе должен быть способен к образованию мостиков (Cl–, Br–, I–, N3–, NCS–, bipy).
Дата добавления: 2020-07-18; просмотров: 140;










