АЛКИЛИРОВАНИЕ СПИРТОВ
Алкилированием называют реакции введения в молекулы органических веществ алкильных радикалов. При введении алкильного радикала в молекулу спирта вместо атома водорода ОН-группы получают простые эфиры. Алкилировать спирты можно спиртами, как это осуществляется при их межмолекулярной дегидратации:

Можно алкилировать спирты галоидными алкилами. Однако спирты являются слабыми нуклеофилами и с галоидными алкилами реагируют чрезвычайно медленно. Если реакцию галоидных алкилов проводить не со спиртами, а с алкоголятами, то простые эфиры образуются быстрее, поскольку алкоголят-ионы – сильные нуклеофилы и алкилирование в этом случае осуществляется очень активно:

метилэтиловый эфир
Алкилировать алкоголяты можно и диалкилсульфатами:

Взаимодействие алкоголятов с алкилгалогенидами является общим методом получения простых эфиров, известным под названием „синтеза Вильямсона”.
Реакция алкоголятов с галогеналкилами осуществляется по SN2 – механизму:

ОКИСЛЕНИЕ СПИРТОВ
Спирты при 300-400оС и в присутствии медных и других катализаторов окисляются кислородом воздуха. Такие окислители, как KMnO4, хромовая смесь, окисляют спирты уже при комнатной температуре. В зависимости от того, какой это спирт – первичный, вторичный или третичный – при окислении образуются разные продукты.
Первичные спирты при окислении дают альдегиды с таким же количеством углеродных атомов, как и в молекуле исходного спирта. Альдегиды в этих условиях могут окисляться в карбоновые кислоты. Чтобы избежать дальнейшего окисления, альдегиды необходимо быстро выводить из реакционной смеси:

альдегид карбоновая кислота
Окисление спиртов хромовой смесью сопровождается изменением оранжево-красного окрашивания реакционной смеси (ионы Cr2O72-) на зеленое (ионы Cr3+):


Первичные спирты можно также окислить в альдегиды мелко раздробленной медью. Нагретой до 280-300оС. В этих условиях от молекулы спирта отщепляются два атома водорода и в молекуле органического вещества, которая при этом образуется, появляется двойная связь углерод – кислород (>C=O). Такое превращение спиртов называется дегидрированием:

Вторичные спирты при окислении, а также при дегидрировании, превращаются в кетоны:

Например, втор-пропиловый спирт в этих условиях превращается в кетон, который называют ацетоном:

Диметилкетон
(ацетон)
Третичные спирты окисляются достаточно трудно с одновременным разрывом углеродной цепи их молекул и образования смеси карбоновых кислот и кетонов. Такое окисление этих спиртов связано с тем, что в условиях реакции окисления они дегидратируются и превращаются в этиленовые углеводороды, которые в присутствии сильного окислителя окисляются с разрывом молекулы по месту двойной С=C - связи.
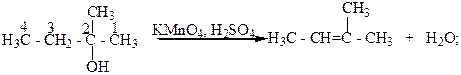
2- Метилбутанол-2 2-Метилбутен-2.
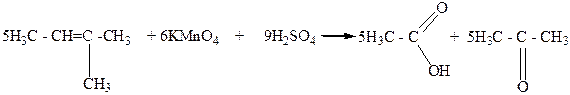
Уксусная Диемтилкетон
кислота (ацетон)
Таким образом, по продуктам окисления спиртов можно сделать вывод о строении спиртов.
Дата добавления: 2022-04-12; просмотров: 375;










