Критическая точка. Равновесие жидкости и газа.
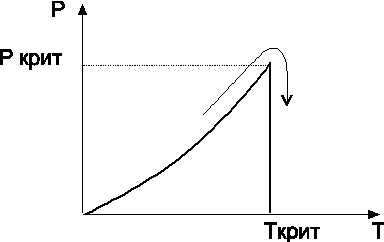
Кривая равновесия фаз p(T)
При переходе через неё состояние тела переходит в другую фазу. На кривой (по определению) – равновесие фаз. По рисунку видно, что эта кривая может обрываться, что существует только для фаз «жидкость-газ» (пар). При p>pкр, T>Tкр двухфазной системы «жидкость-газ» нет.
Как поведёт себя кривая равновесия на плоскостях (T,V), (p,V)? Ясно, что при одной и той же температуре объём может быть разным при равновесии фаз, и кривой p(T) соответствует целая (заштрихованная) область на этих плоскостях.
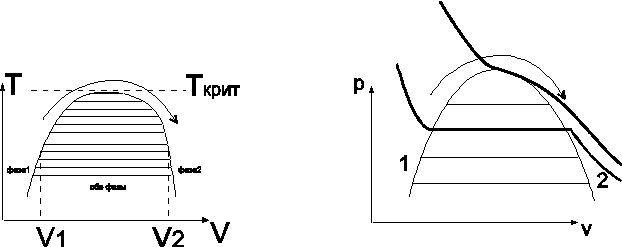
При приближении температуры к Tкр удельные объёмы находящихся в равновесии фаз сближаются и в критической точке совпадают (удельный вес одинаковый). То же самое про давление. При достижении критической точки между двумя состояниями вещества может быть осуществлён непрерывный переход, при котором ни в какой момент не происходит расслоение на фазы (нет резкой границы). Для этого надо менять состояние вдоль кривой (какой-нибудь), огибающей критическую точку и нигде не пересекающей кривую равновесия. Таким образом, понятие о различных фазах ограничивается условием, оно имеет смысл только в случае, когда обе одновременно существуют (на кривой равновесия). Ясно, что критическая точка может существовать только таких фаз, различие между которыми носит чисто качественный характер – жидкость и газ, жидкость и твёрдое тело, газ и твёрдое тело и т.д. Они отличаются между собой различной симметрией
Параметры для воды:
Tкр=220°С, pкр=220 атм.
Определим теперь соотношение масс и объёма, например, на кривой T(V) (см. на рис.). В точке 1 – всё жидкость (объём V1), В точке 2 – всё газ (объём V2). Общий объём V. Каково соотношение масс?
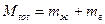
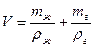
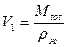
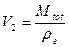
Теперь вычислим:
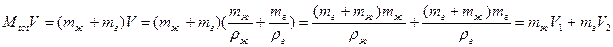
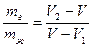 - похоже на правило рычага.
- похоже на правило рычага.
Дата добавления: 2021-05-28; просмотров: 213;










