ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ
Термодинамикаизучает законы, которые описывают энергетические превращения, сопровождающие физические, химические и биологические процессы.
Переходы энергии из одной формы в другую, энергетические эффекты, сопровождающие различные химические реакции, а также условия самопроизвольного протекания процессов и пределы их протекания в данных условиях – всё это является предметом изучения науки, называемой химической термодинамикой.
Одним из основных понятий в термодинамике является физико-химическая система (или просто система)[*] – тело или группа взаимодействующих тел, фактически или мысленно выделяемых из окружающей среды.
Гомогенная система – однородная система, в которой нет частей, различающихся по свойствам и разделённых поверхностями (границами) раздела. Например, воздух, вода, истинные растворы.
Гетерогенная система – разнородная система, состоящая из двух или более частей, отличающихся по свойствам, между которыми есть поверхность раздела, где свойства системы резко меняются (скачком). Например, молоко, кровь, смеси воды и льда, воды и масла.
Часть гетерогенной системы, которая имеет одинаковые свойства и отделённая поверхностью раздела, называется фазой. Например, в молоке имеются три фазы: водная (жидкая) фаза – раствор солей, углеводов, белков и других веществ, в которой распределены две другие фазы: мельчайшие капельки жидких жиров и мельчайшие частички твёрдых жиров, (твердая фаза).
Живые системы, существующие на Земле, — гетерогенны. Они всегда отделены от окружающей среды оболочкой, кроме того, внутри каждой живой клетки имеется множество различных мембран – границ между её частями.
В зависимости от характера взаимодействия с окружающей средой различают системы изолированные, закрытые (замкнутые) и открытые.
Изолированная система характеризуется отсутствием обмена энергией и веществом с окружающей средой. Например, термос.
Закрытая система обменивается с окружающей средой энергией, а обмен веществом исключён. Например, закупоренная бутылка, попеременно помещаемая в горячую и холодную воду, будет получать и отдавать энергию, но масса содержимого бутылки будет оставаться постоянной.
Открытая система обменивается с окружающей средой энергией и веществом. Например, кипящая в кастрюле вода получает энергию от плиты, а при испарении теряет часть своей энергии и массы.
Живой организм представляет собой открытую систему, жизнедеятельность которой невозможна без постоянного обмена веществом, и энергией с окружающей средой. Абсолютно изолированных систем в природе нет.
В термодинамике принято различать три состояния системы: равновесное, стационарное и переходное.
Термодинамически равновесное состояние системы характеризуется постоянством свойств во времени в любой её точке и отсутствием потоков вещества и энергии.
Термодинамически равновесное состояние системы — это прежде всего устойчивое состояние системы. Для выведения системы из этого состояния необходим обмен энергией или веществом между системой и окружающей средой. Важно различать состояния термодинамического равновесия и химического равновесия; последнее всегда имеет динамический характер, так как достигается в результате выравнивания скоростей обратимых процессов.
Стационарное состояние системы характеризуется постоянством свойств во времени, которое поддерживается за счёт непрерывного обмена веществом и энергией между системой и окружающей средой.
Для живого организма характерно стационарное состояние, а не равновесное, означающее для него смерть, так как прекращаются потоки вещества, энергии и информации между окружающей средой и организмом, обеспечивающие его жизнедеятельность.
Когда система переходит из одного (равновесного или стационарного) состояния в другое, то она находится в переходном состоянии.
Переходное состояние характеризуется изменением свойств системы во времени.
Состояние системы характеризуется определённой совокупностью физических и химических величин – параметров системы, к которым относятся: масса (m), количество вещества ( n), объём (V), температура (Т), давление (р), концентрация (с). Значение параметра можно измерить непосредственно.
Параметры системы разделяют на экстенсивные и интенсивные.
Значенияэкстенсивных параметров пропорциональны числу частиц в системе (m, n, V).
Значения интенсивных параметров не зависят от числа частиц в системе (T, p, c).
Различие экстенсивных и интенсивных параметров чётко проявляется при взаимодействии систем: значения экстенсивных параметров суммируются, а интенсивных – усредняются.
Для характеристики состояния системы, наряду с параметрами, используют функции состояния. Их значения рассчитывают по соответствующим математическим формулам, исходя из значений параметров, описывающих данное состояние системы. Функцией состояния системы, например, является энергия.
Функции состояния системы - экстенсивные величины.
Значения параметров и функций состояния системы определяются только состоянием системы. Поэтому при переходе системы из одного состояния в другое изменения (Δ) этих величин не зависят от пути перехода, а определяется лишь начальным и конечным состояниями системы, то есть их значениями в этих состояниях.
Δ = 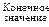
 –
– 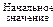

Переход системы из одного состояния в другое, сопровождающийся необратимым или обратимым изменением хотя бы одного параметра, характеризующего данную систему, называется процессом.
В отличие от состояния системы, которое характеризуется значениям и существующих параметров или функции, характеристикой процесса является их изменение, то есть значение Δ.
Процессы, в зависимости от изменения параметров системы, разделяют на изотермические, изобарические, изохорические:
изотермический процесс Т = const, DТ = 0;
изобарический процесс р = const, Dр = 0;
изохорический процесс V = const, DV = 0.
Жизнедеятельность человека протекает при постоянстве температуры и давления, то есть при изобарно-изотермических условиях (р, Т = const).
Для описания движения материи в живых организмах, по мнению В.И. Слесарёва, необходимо знать значения трёх функций состояния: энергии, энтропии и информации.
Энергия (Е) – количественная мера интенсивности различных форм перемещения и взаимодействия частей в системы, включая перемещение системы в целом и её взаимодействие с окружающей средой. Единица энергии – кДж/моль
В зависимости от формы движения материи различают тепловую, электрическую, химическую, ядерную и другие виды энергии. Термодинамика рассматривает превращение тепловой энергии в другие виды энергии – механическую, химическую, электрическую и т. д.
Движение материи включает перемещение частей системы, которое характеризуется кинетической энергией (Екин), и взаимодействие частей системы, которое характеризуется потенциальной энергией (Епот).
Энергетическое состояние системы описывается такой функцией состояния, как внутренняя энергия.
Внутренняя энергия (U) представляет собой полную энергию системы, которая равна сумме потенциальной и кинетической энергии частей данной системы, в том числе на молекулярном, атомарном и субатомарном уровнях:
U = Екин + Епот.
Внутренняя энергия не включает потенциальную энергию, обусловленную положением системы в пространстве, и кинетическую энергию движения системы в целом.
Внутренняя кинетическая энергия обусловлена тепловым хаотическим движением химических частиц (атомов,молекул,) = что непосредственно связано с температурой – с увеличением интенсивности этого движения температура тела возрастает.
Внутренняя потенциальная энергия системы обусловлена взаимодействием химических частиц друг с другом.
Значение внутренней энергии определить невозможно, так как любая термодинамическая система материальна, а материя неисчерпаема. Экспериментально можно определить изменение внутренней энергии (DU) при взаимодействии системы с окружающей средой, если обмен энергией осуществляеться в виде работы и теплоты.
Работа (А) – энергетическая мера направленных форм движения частей системы в процессе её взаимодействия системы с окружающей средой.
Работа в термодинамике считается положительной (А > 0), когда она совершается системой против внешних сил окружающей среды, при этом внутренняя энергия системы уменьшается (∆U < 0).
Теплота (Q) – энергетическая мера хаотических форм движения частей системы в процессе её взаимодействия системы с окружающей средой.
В термодинамике теплота считается положительной (Q > 0), если она сообщается системе из окружающей среды, при этом внутренняя энергия системы увеличивается (∆U > 0).
Работа и теплота не являются свойствами системы, а характеризуют процесс обмена энергией системы с окружающей средой, поэтому их величины зависят от пути процесса, по которому система переходит из одного состояния в другое.
Термины "работа" и "теплота" означают как сам процесс передачи энергии, так и величину передаваемой при этом энергии.
Для характеристики движения частей системы в термодинамике, наряду с энергией, используется ещё одна функция состояния – энтропия.
Энтропия (S) – термодинамическая функция, характеризующая меру неупорядоченности системы, то есть неоднородности расположения и движения её частей.
Изменение энтропии системы в условиях термодинамически обратимого процесса равно отношению передаваемой теплоты к температуре, при которой осуществляется этот процесс:
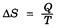
Единица энтропии – Дж/(моль∙К).
Факторы, влияющие на величину энтропии, описаны в разд. 3.
Энтропия является экстенсивным свойством системы, поэтому её изменение в результате какого-либо процесса равно разности энтропий конечного и начального состояний системы, независимо от пути процесса:
DS = Sкон – Sнач.
Движение материи невозможно описать без таких термодинамических характеристик, как энергия и энтропия. Если энергия количественно характеризует интенсивность движения и взаимодействия частей системы, то энтропия – мера неупорядоченности системы, то есть расположения и движения её частей. Изменение энтропии при превращения энергии из одного вида в другой характеризует величину рассеяния энергии при этом процессе. Чем больше DS, тем меньше коэффициент полезного действия (КПД) процесса. Именно этим объясняется низкий КПД (~ 40 %) при превращении тепловой энергии в электрическую. В то же время в гальваническом элементе, где химическая энергия окислительно-восстановительной реакции превращается в электрическую, КПД может достигать 98 %. В первом случае хаотическое движение частей системы необходимо превратить в направленное, при этом происходит сильное изменение энтропии. Во втором случае направленное движение электронов и ионов, сопровождающее химическую реакцию, превращается в направленное движение заряженных частиц, то есть упорядоченность движения частиц сохраняется, и поэтому изменение энтропии незначительно, а следовательно, и рассеяние энергии незначительно.
Для полной характеристики движения частей системы наряду с энергией и энтропией вводится такая функция состояния системы, как информация.
Информация (I О.Ш)– мера организованности системы, то есть упорядоченности расположения и движения её частей.
Информация выражается в битах, причём 1 бит информации эквивалентен 10–23 Дж/К, то есть является очень малой величиной.
Энтропия и информация являются статистическими характеристиками движения, описывающими его с противоположных сторон.
Для самоорганизующихся систем наряду с законами сохранения массы, электрического заряда, энергии (разд. 2) выполняется ещё закон сохранения:
I + S = const.
При этом, обе величины измеряются в одинаковых единицах, а значение их суммы зависит от типа системы. Это соотношение означает, что энтропия есть мера недостатка информации. При возрастании I убывает S и наоборот. Физический смысл этого закона: за полученную информацию система платит уменьшением энтропии, поэтому получение системой любой информации всегда связано с возрастанием энтропии в окружающей среде. Живые организмы – это высокоупорядоченные системы, содержащие колоссальное количество информации и, соответственно, обеднённые энтропией. Понятие "информация системы" тесно связано со структурой системы, поэтому целесообразно для характеристики соответствующих систем (нуклеиновые кислоты, белки, водные растворы) использовать термин "структурно-информационные свойства".
2. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Первый закон (первое начало) термодинамики – это всеобщий закон природы – закон сохранения и превращения энергии, соответствующий основному положению диалектического материализма о вечности и неуничтожимости движения.
Энергия не исчезает и не возникает из ничего, а только превращается из одного вида в другой в эквивалентных соотношениях.
Впервые этот закон в 1842 г. сформулировал немецкий физик Ю. Мейер, врач по образованию.
В зависимости от типа системы I закон термодинамики имеет различные формулировки.
В изолированной системе её внутренняя энергия постоянна (∆U = 0).
Для закрытой системы I закон – термодинамики устанавливает связь между теплотой, получаемой или выделяемой системой в некотором процессе, изменением её внутренней энергии и произведённой при этом работой.
Если к закрытой системе подвести теплоту Q, то она расходуется на увеличение внутренней энергии этой системы DU и на совершение ею работы против внешних сил окружающей среды:
Q= DU + А.
В изобарно-изотермических условиях, в которых функционируют живые организмы, совершаемая работа А = pDV, тогда:
Q = DU + pDV = (Uкон - Uнач) + (pVкон - pVнач) =
= (Uкон + pVкон) – (Uнач + pVнач)
Сумму внутренней энергии системы и произведения объёма на давление (U + pV) называют теплосодержанием, или энтальпией системы*.
Энтальпия (Н)– термодинамическая функция, характеризующая энергетическое состояние системы при изобарно-изотермических условиях.
Раздел химии, занимающийся изучением тепловых эффектов химических реакций, называется термохимией.
Теплота, полученная системой при р, Т = const, равна приращению энтальпии системы DН:
Q = Hкон – Ннач = DН.
Величину энтальпии системы, как и абсолютную величину её внутренней энергии системы, определить невозможно, поэтому в термодинамических расчётах используется лишь изменение энтальпии, происходящее при переходе системы из одного состояния в другое. Величина DН системы не зависит от пути процесса, а определяется, как и для любой другой функции состояния, разностью энтальпий, характеризующих конечное и начальное состояния системы:
DН = Hкон – Ннач.
Количество теплоты, которое выделяется или поглощается при прохождении химической реакции в изобарно-изотермических условиях, характеризуется изменением энтальпии системы и называется энтальпией реакции(DНр).
Химические процессы (химические реакции) и физико-химические процессы подразделяются на экзотермические и эндотермические.
Экзотермические процессы сопровождаются выделением энергии из системы в окружающую среду.
В результате экзотермических процессов энтальпия системы уменьшается (Нкон < Hнач), следовательно:
DНэкзо = (Нкон - Hнач ) < 0.
Эндотермические процессы сопровождаются поглощением энергии системой из окружающей среды.
В результате эндотермических процессов энтальпия системы увеличивается (Hкон > Hнач), следовательно:
DНэндо = (Нкон - Hнач ) > 0.
Энтальпия системы является, как и другие функции системы экстенсивной функций и зависит от количества вещества, температуры и давления, поэтому изменение энтальпии в результате химической реакции физико-химических процессов определяется при стандартных условиях.
Стандартные условия: количество вещества - 1 моль;
давление - 760 мм рт. ст. 101 325 Па (1 физическая атмосфера ,или 760 мм рт.ст.)
температура - 298 К или 25 °С.
Термодинамические параметры и функции состояния системы и их изменения, определённые измеренные при стандартных условиях, обозначаются соответствующим символом с верхним индексом "°". Стандартную энтальпию реакции обозначают 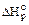 , кДж/моль.
, кДж/моль.
Стандартная энтальпия химической реакции представляет собой энергетическую характеристику реакции, проводимой при стандартных условиях. Уравнения химических реакций, в которых указано значение энтальпии, называются термохимическими уравнениями. Например, для реакции окисления процесса сгорания 1 моль ацетилена:
С2Н2(г) + 2,5О2(г) = 2СО2(г) + Н2О(г); = - 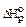 1256 кДж/моль.
1256 кДж/моль.
Кроме теплового эффекта в термохимических уравнениях указывают индексы, обозначающие агрегатные состояния реагирующих веществ. Стехиометрические коэффициенты могут иметь дробные; это связано с тем, что тепловой эффект реакции рассчитывается на 1 моль продукта реакции или на 1 моль одного из реагирующих веществ.
Для оценки энергетического состояния веществ используются значения их стандартных энтальпий образования, обозначаемые ∆Н°[вещество (агрегатное состояние)], кДж/моль.
Стандартная энтальпия образования простых веществ в их наиболее термодинамически устойчивом агрегатном и аллотропном состоянии при стандартных условиях принимается равной нулю.
Например, для кислорода DНо (О2) = 0, для графита 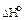 (Сграфит) = 0. Однако стандартная энтальпия образования озона DHо (О3) = 142,2 кДж/моль, алмаза DНо (Салмаз) = 1,8 кДж/моль.
(Сграфит) = 0. Однако стандартная энтальпия образования озона DHо (О3) = 142,2 кДж/моль, алмаза DНо (Салмаз) = 1,8 кДж/моль.
Стандартная энтальпия образования сложного вещества равна энтальпии реакции получения 1 моль этого вещества из простых веществ при стандартных условиях.
Например, стандартная энтальпия образования этанола равна стандартной энтальпии гипотетической реакции:
2Сграфит + 3Н2(г) + 0,5О2 (г) = С2Н5ОН(ж);
DНо (С2Н5ОН) = -277 кДж/моль.
Значение стандартной энтальпии образования сложного вещества зависит от его природы и агрегатного состояния. Числовые значения стандартных энтальпий образования веществ приводятся в справочниках.
Энтальпию химической реакции можно определить как экспериментально, так и методами расчёта с использованием стандартных энтальпий образования реагирующих веществ веществ, в химической , на основе закона, открытого Г. И. Гессом (1840 г.).
Энтальпия, или тепловой эффект химической реакции, зависит от природы и состояния исходных веществ и конечных веществ и не зависит от пути, по которому протекает данная реакция.
Закон Гесса является вполне строгим для процессов, происходящих при постоянном давлении или при постоянном объёме. Для этих процессов он может рассматриваться как частная форма выражения закона сохранения энергии применительно к химическим реакциям.
| Герман Иванович Гесс (7.VIII 1802—12.XII 1850). Русский химик, академик Петербургской АН (с 1830). Родился в Женеве 7 августа 1802 г. Окончил Дерптский университет (доктор медицины, 1825). Совершенствовал образование в Стокгольмском университете (1825). С 1830 – профессор Петербургского технологического института, в 1832–1849 –Петербургского горного института.Один из основоположников термохимии. Значительно раньше J. П. Ю. Ю. Томсена и П. Э. М. Бертло выдвинул (1840) положение, согласно которому величины тепловых эффектов реакции могут служить мерой химического сродства. | 
|
Открыл (1840) основной закон термохимии – закон постоянства количества теплоты, по которому тепловой эффект реакции зависит только от начального и конечного состояния реагирующих веществ, а не от количества её стадий (закон Гесса). Доказал (1842), что при смешении нейтральных солевых растворов тепловой эффект отсутствует (правило термонейтральности). Установил, что при нейтрализации эквивалента сильной кислоты сильным основанием выделяется одинаковое количество теплоты (13,5 ккал). Открыл и определил (1830–1834) состав четырех новых минералов – вертита, уваровита, гидроборацита и фольбортита. Предложил (1833) способ получения теллура из теллурида серебра — минерала, который был им впервые изучен. Изучал (1832) оксиды кобальта. Установил каталитические и адсорбционные свойства мелкораздробленной платины. Одним из первых изучал состав кавказских нефтей. Открыл сахарную кислоту. Написал учебник «Основания чистой химии» (1831), выдержавший семь изданий.
В честь Г.И.Гесса теллурид серебра назван гесситом.
Закон Гесса можно проиллюстрировать следующей схемой:
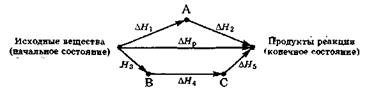
Переход системы из начального состояния в конечное можно осуществить разными путями:
= непосредственно химической реакцией, энтальпия которой равна DHр;
= в результате двухстадийной реакции через промежуточное состояние А в результате двухстадийной реакции, энтальпии отдельных стадий которой равны DH1 и DH2;
= в результате трёхстадийной реакций через промежуточные состояния В и С в результате трёхстадийной реакций, энтальпии отдельных стадий которой равны DH3, DH4 и DH5.
Согласно закону Гесса:
DHр = DH1 + DH2 = DH3 + DH4 + DH5.
В термохимических расчётах большое значение имеют следствия из закона Гесса.
Первое следствие. Энтальпия химической реакции равна разности алгебраических сумм энтальпий образования продуктов реакции и исходных веществ:
DHр = ∑vкон DHкон (Yкон) - ∑vисх DHисх (Xисх),
где DH (Y), DH (X) - энтальпии образования продуктов реакции Y и исходных веществ X;
vкон. и vнач - соответствующие стехиометрические коэффициенты в уравнении химической реакции.
Например, для реакции образования хлороводорода
Н2 + Cl2 = НCl
энтальпия реакции равна
DHр = 2DH (НCl) – [DH (Н2) + DH (Cl2)
Первое следствие позволяет определять энтальпии различных химических реакций (в том числе и биохимических, осуществление которых in vitro* невозможно), используя табличные значения стандартных энтальпий образования исходных веществ и продуктов реакции.
Рассчитаем, например, энтальпию реакции получения мочевины в организме из аммиака и оксида углерода (IV):
2NH3(г) + СО2(г) = СО(NH2)2(т) + Н2О(г)
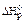 = [
= [  (СО(NH2)2(т) +
(СО(NH2)2(т) +  ( Н2О(г))] – [2
( Н2О(г))] – [2  ( NH3(г) +
( NH3(г) +  ( СО2(г)) =
( СО2(г)) =
= (–333 – 242) – (–2 ∙ 46 – 394) = 89 кДж/моль.
Второе следствие Энтальпия прямой реакции численно равна энтальпии обратной реакции, но с противоположным знаком:
∆ 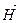 = – ∆
= – ∆ 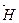 .
.
Рассчитаем, например, стандартную энтальпию реакции фотосинтеза глюкозы, которая является обратной реакцией окисления (горения) глюкозы:
6СО2(г) + 6Н2О(ж) 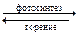 С6Н12О6(т) + 6О2(г)
С6Н12О6(т) + 6О2(г)
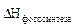 = –
= – 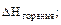
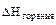 (С6Н12О6(т)) = – 1273 кДж/моль.
(С6Н12О6(т)) = – 1273 кДж/моль.
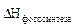 (С6Н12О6(т)) = – (– 1273) = 1273 кДж/моль.
(С6Н12О6(т)) = – (– 1273) = 1273 кДж/моль.
Основным источником энергии для живых организмов является химическая энергия, заключённая в продуктах питания. Для человека главными компонентами пищи являются жиры, углеводы сахара и белки, окисление которых сопровождается выделением энергии. В медицине энергетическую характеристику продуктов питания принято выражать в калориях. Пища представляет собой смесь питательных веществ сложного состава, поэтому калорийность пищи указывается в расчёте на 1 г, а не на 1 моль.
Калорийностью питательных веществ называется энергия, выделяемая при полном окислении (сгорании) 1 г этих веществ.
Взаимосвязь между единицами энергии выражается соотношением: 1 калория = 4,18 Дж.
Согласно закону Гесса теплота, которая выделяется при окислении питательных веществ, не зависит от того, как или где они окисляются, конечно, при условии, что продукты реакции остаются неизменными. Жиры, углеводы и белки окисляются в организме до тех же продуктов, что и при сгорании в калориметре:
“С” 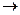 СO2; “Н”
СO2; “Н” 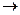 Н2О; “N”
Н2О; “N” 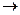 N2*
N2*
Поэтому для энергетической оценки большинства продуктов питания может служить энтальпия реакции их сгорания. Наибольшую энергетическую ценность имеют жиры, при окислении которых выделяется 37,7=39,8 кДж/г (9,0=9,5 ккал/г). В процессе усвоения углеводов в организме человека выделяется 16,5=17,2 кДж/моль (4,0=4,1 ккал/г). На этом же уровне находится и калорийность белков: 16,5=17,2 кДж/г (4,0=4,1 ккал/г). Биоэнергетику организма можно регулировать не только при помощи выбора отдельных продуктов, но, главным образом, их сочетанием. Для взрослого человека суточная норма потребления составляет: жиров – 60=70 г, белков – 80=100 г (при тяжёлом физическом труде – 130=140 г), а потребляемая масса углеводов должна в 4=5 раз превышать массу белков, причём только небольшая часть от этого количества должна быть в виде сахарозы (около 8 г).
В основе научной диетологии лежит соответствие калорийности пищевого рациона энергозатратам человека. Суточная потребность человека в энергии составляет:
8 400=11 700 кДж (2 000=2 800 ккал) при лёгкой работе в сидячем положении (портные, канцелярские работники);
12 500=15 100 кДж (3 000=3 600 ккал) при умеренной и напряженной мышечной работе (учащиеся, студенты, врачи, рабочие-станочники);
16 700=20 900 кДж (4 000=5 000 ккал) при тяжёлом физическом труде (литейщики, кузнецы)
до 30 100 кДж (7 200 ккал) при особо тяжёлом труде (землекопы, косари, спортсмены).
3. ПОНЯТИЕ О САМОПРОИЗВОЛЬНЫХ ПРОЦЕССАХ. ЭНТРОПИЯ
Одним из важнейших аспектов термодинамики является формулировка условий самопроизвольности протекания химических и физико-химических процессов.
Самопроизвольным (или спонтанным) является процесс, который совершается в системе без затраты работы извне и который уменьшает работоспособность системы после его завершения.
Следовательно, самопроизвольно система может переходить только из менее устойчивого состояния в более устойчивое. На основе I закона термодинамики можно сформулировать один из важных принципов самопроизвольности протекания процессов в системе, заключающийся в стремлении системы к минимуму энергии за счёт выделения энергии в окружающую среду.
Этот энергетический принцип особенно важен для систем, которые можно рассматривать как единую частицу.
Например, капля дождя самопроизвольно падает вниз, уменьшая при этом свою потенциальную энергию. Каплю воды необходимо рассматривать как совокупность большого числа молекул, когда происходит процесс её испарения, протекающий самопроизвольно, несмотря на то, что он как эндотермический процесс требует поступления энергии из окружающей среды.
Следовательно, для описания условий протекания самопроизвольных процессов одного энергетического принципа недостаточно, особенно в системах, состоящих из большого числа частиц. Главное изменение, которое происходит при испарении капли, заключается в переходе системы из жидкого состояния (с частично упорядоченным состоянием частиц) в парообразное, в котором частицы не упорядочены. Таким образом, для описания движения в системах, содержащих большое число частиц, необходимо учитывать неупорядоченность расположения и движения этих частиц, то есть энтропию системы (разд. 1).
Значение энтропии как меры неупорядоченности системы зависит от агрегатного состояния и природы веществ (компонентов системы), температуры, давления и сложности данной системы.
Энтропия вещества в газообразном состоянии больше, чем энтропия его в жидком состоянии, а последняя больше энтропии этого вещества в твёрдом состоянии:
S(г) > S(ж) > S(т).
Энтропия простых веществ зависит от их аллотропной модификации:
S(Сграфит) > S(Салмаз); S(О2) < S(О3).
Энтропия системы при повышении температуры возрастает, так как увеличивается неупорядоченность движения частиц:
если Т2 > Т1, то S2 > S1.
Энтропия системы при повышении давления уменьшается, так как снижается неупорядоченность движения частиц:
если p2 > р1, то S2 < S1.
Энтропия системы с увеличением её сложности повышается, так как возрастает число типов частиц и вариантов их расположения.
Для энергетической характеристики веществ при стандартных условиях, наряду со стандартной энтальпией, используют и их стандартную энтропию Sо. В отличие от стандартной энтальпии, стандартная энтропия простых веществ не равна нулю.
В случае идеально упорядоченного кристалла при температуре 0 К его энтропия S = 0. Это даёт естественную нулевую точку отсчёта для значений энтропии (отсутствующую для ранее рассмотренных функций состояния: внутренней энергии U и энтальпии Н) и позволяет измерить или теоретически рассчитать значения энтропии. Поэтому перед символом энтропии веществ не ставят знак изменения (D-дельта). Значения энтропии для стандартных состояний веществ приведены в справочниках термодинамических величин.
Изменение стандартной энтропии в химической реакции (  ) определяется разностью алгебраических сумм стандартных энтропии продуктов реакции Yкон. и исходных веществ Хисх. с учётом соответствующих стехиометрических коэффициентов:
) определяется разностью алгебраических сумм стандартных энтропии продуктов реакции Yкон. и исходных веществ Хисх. с учётом соответствующих стехиометрических коэффициентов:
DSр = ∑vкон DSкон (Yкон) - ∑vисх DSисх (Xисх),
где DS (Y), DS (X) - энтропии образования продуктов реакции Y и
исходных веществ X;
vкон.. и vнач.- соответствующие стехиометрические коэффициенты
в уравнении химической реакции.
4. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ.
ЭНЕРГИЯ ГИББСА
Второй закон (второе начало) термодинамики определяет направленность и пределы протекания самопроизвольных химических и физико-химических процессов, в том числе и биохимических.
Рассмотрим изолированную систему, где исключён обмен энергией и веществом. Допустим, что в изолированной системе находятся два любых газа, например гелий Не и аргон Аr, которые химически и физически не взаимодействуют между собой и не перемешаны. Естественно, что эти газы будут самопроизвольно и необратимо смешиваться, однако свойства системы останутся без изменения, за исключением её энтропии. В исходном состоянии системы, когда газы ещё не смешались, её энтропия (Sнач) меньше, чем после смешивания газов (Sкон), характеризующегося неупорядоченностью расположения и движения молекул газов. Следовательно, в результате самопроизвольного необратимого процесса в изолированной системе её энтропия возростает: DS = Sкон - Sнач > 0. отсюда сформулирован II закон термодинамики гласит для изолированных систем.
В изолированных системах самопроизвольно могут совершаться только такие необратимые процессы, при которых энтропия системы возрастает (DS > 0).
Для неизолированных систем нужно учитывать не только изменение энтропии, но и изменение энергии. Поэтому необходимо рассматривать две тенденции, определяющие направление самопроизвольно протекающих процессов:
= стремление системы к достижению минимума энергии;
= стремление системы к максимуму энтропии, то есть к
неупорядоченности.
Процессы, при которых энергия в неизолированной системе уменьшается, а энтропия возрастает, протекают самопроизвольно. Самопроизвольность других процессов зависит от того, какая из этих двух тенденций – энергетическая или энтропийная – окажется более эффективной, какая из этих противоборствующих тенденций получит перевес над другой. В этом проявляется противоречивость материального мира.
Для однозначной формулировки условий протекания самопроизвольных процессов в любых системах введена ещё одна термодинамическая функция, которая характеризует одновременно и энергетику, и неупорядоченность систем. Впервые такую термодинамическую функцию ввёл Д. У. Гиббс, и в память об этом выдающемся американском учёном её назвали энергией Гиббса.
| Джозайя Уиллард Гиббс (11.11 1839=28. IV 1903). Американский физик и физико-химик, член Национальной АН США (с 1879). Родился 11 февраля в Нью-Хейвене. Окончил Йельский университет (1858; доктор философии, 1863). В 1863=1866 преподавал в Йельском колледже. Совершенствовал образование в Сорбонне и Коллеж де Франс в Париже (1866=1867), в Берлинском (1867) и Гейдельбергском (1868) университетах. С 1871 – профессор Йельского университета. Один из основоположников термодинамики. | 
|
Предложил (1873) графические модели описания термодинамических свойств веществ. Разработал (1875=1878) теорию термодинамических потенциалов, изучил (1875) условия равновесия гетерогенных систем. Вывел (1875=1878) правило фаз, согласно которому в равновесной гетерогенной системе число фаз не может превышать числа компонентов системы, увеличенного на два. Предложил (1878) графическое изображение состояния трёхкомпонентной системы (треугольник Гиббса). Заложил основы термодинамики поверхностных явлений и электрохимических процессов; ввёл понятие адсорбции. Дал (1902) атомистическое истолкование развитым им термодинамическим методам. Осу
Дата добавления: 2016-12-09; просмотров: 3629;










