ХИМИЧЕСКИЕ СВОЙСТВА
Химические свойства гликолей аналогичны свойствам одноатомных спиртов и определяется присутствием в их молекулах двух гидроксильных групп. Причем в реакциях могут принимать участие одна или обе гидроксильные группы. Однако вследствие взаимного влияния одной гидроксильной группы на другую (особенно у α-гликолей) кислотно-основные свойства гликолей несколько отличаются от аналогичных свойств одноатомных спиртов. В связи с тем, что гидроксил проявляет отрицательный индукционный эффект, одна гидроксильная группа оттягивает электронную плотность от другой аналогично тому, как это делает атом галогена в молекулах замещенных одноатомных спиртов. В результате такого влияния кислотные свойства двухатомных спиртов по сравнению с одноатомными повышаются:



 Н-О СН2 СН2 О Н
Н-О СН2 СН2 О Н
Поэтому гликоли, в отличие от одноатомных спиртов, легко вступают в реакцию не только со щелочными металлами, но и со щелочами и даже с гидроксидами тяжелых металлов. Со щелочными металлами, щелочами гликоли образуют полные и неполные алкоголяты (гликоляты):

С гидроксидами некоторых тяжелых металлов, например с гидроксидом меди, гликоли образуют комплексные гликоляты. При этом нерастворимый в воде Cu(OH)2 в гликоле легко растворяется:

Медь в этом комплексе образует с атомами кислорода две ковалентные связи и две – координационные. Реакция является качественной на двухатомные спирты.
Гликоли могут образовывать полные и неполные простые и сложные эфиры. Так, при взаимодействии неполного гликолята щелочного металла с галоидными алкилами получают неполные простые эфиры, а из полного гликолята – полный простой эфир:
| Моноэтиловый эфир этиленгликоля
этилцеллозольв
| |


| |
| | | Д Диэтиловый эфир этиленгликоля
| |
Метил- и этилцеллозольвы применяют в качестве растворителя в производстве лаков, бездымного пороха (пироксилина), ацетатного шелка и т.д.
С органическими и минеральными кислотами двухатомные спирты образуют два ряда сложных эфиров:

Мононитрат этиленгликоля Динитрат этиленгликоля
Динитрат этиленгликоля – сильное взрывчатое вещество, которое используют вместо нитроглицерина.
Окисление гликолей осуществляется ступенчато, с участием одной или обеих гидроксильных групп одновременно с образованием следующих продуктов:

Двухатомные спирты вступают в реакцию дегидратации. Причем α-, β- и γ-гликоли, в зависимости от условий реакций, по-разному отщепляют воду. Отщепление воды от гликолей может осуществляться внутри- и межмолекулярно. Например:
Внутримолекулярное отщепление воды:
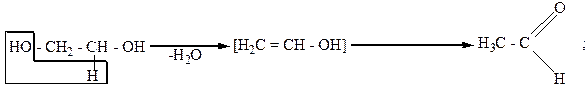

Межмолекулярное отщепление воды.
В 1906 г. А. Е. Фаворский, перегоняя этиленгликоль с серной кислотой, получил циклический простой эфир-диоксан:

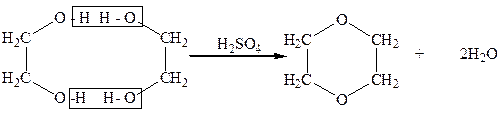
 Диоксан
Диоксан
Диоксан – жидкость, которая кипит при 101оС, смешивается с водой в любых соотношениях, применяется как растворитель и как полупродукт в некоторых синтезах.
При межмолекулярном отщеплении воды от гликолей могут образовываться оксиэфиры (спиртоэфиры), как, например, диэтиленгликоль:

Диэтиленгликоль
 Диэтиленгликоль получают также взаимодействием этиленгликоля с оксидом этилена:
Диэтиленгликоль получают также взаимодействием этиленгликоля с оксидом этилена:
Диэтиленгликоль – жидкость с температурой кипения 245,5оС; используется как растворитель, для заполнения гидравлических приборов, а также в текстильной промышленности.
Широкое применение как хороший растворитель нашел диметиловый эфир диэтиленгликоля (диглим) Н3С-О-СН2-СН2-О-СН2-СН2-О-СН3.
Этиленгликоль при нагревании с оксидом этилена в присутствии катализаторов образует вязкие жидкости – полиэтиленгликоли:
 Полиэтиленгликоль
Полиэтиленгликоль
Полигликоли используются как компоненты разных синтетических моющих средств.
Широкое применение получили полиэфиры этиленгликоля с двухосновными кислотами, которые используются в производстве синтетических волокон, например лавсана (название „лавсан” образовано из начальных букв следующих слов – лаборатория высокомолекулярных соединений Академии наук):
| Диемтиловый эфир терефталевой кислоты
| |


С метанолом терефталиевая кислота образует диметиловый эфир (диметилтерефталат, Ткип.=140оС), который далее путем переэтерификации превращается в этиленгликольтерефталат. При поликонденсации этиленгликольтерефталата образуется полиэтилентерефталат с молекулярной массой 15000-20000. Волокно лавсан не мнется, устойчиво к разным погодным условиям.
Дата добавления: 2022-04-12; просмотров: 186;



 Н-О СН2 СН2 О Н
Н-О СН2 СН2 О Н





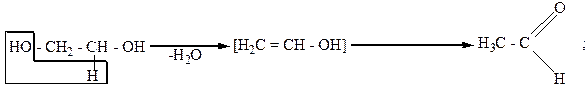


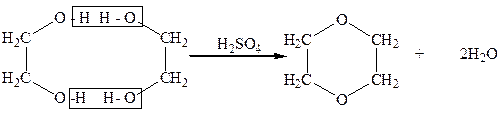
 Диоксан
Диоксан
 Диэтиленгликоль получают также взаимодействием этиленгликоля с оксидом этилена:
Диэтиленгликоль получают также взаимодействием этиленгликоля с оксидом этилена: Полиэтиленгликоль
Полиэтиленгликоль











