Уравнения изопроцессов
Изопроцессами называются такие процессы, в которых какое-либо условие или параметр поддерживаются постоянными.
К характерным изопроцессам относятся следующие:
1. Изотермический. Это обратимый процесс, проходящий при постоянной температуре (газ в термостате): Т = const = Т0. Для него уравнение состояния идеального газа принимает вид:
pV = νRT0 = const. (4.1)
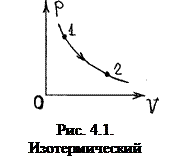
Это уравнение изотермы. Его график – это симметричная гипербола (рис. 4.1). Для любых двух точек на изотерме p1V1 = p2V2.
2. Изохорный процесс. Это обратимый процесс, протекающий при постоянном объёме, т. е. в баллоне с жёсткими стенками: V = const = V0. Для него уравнение состояния pV = νRT примет вид:
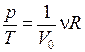 = const.
= const.
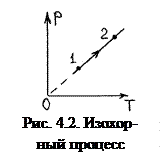
Это уравнение изохоры. На изохоре р1 /T1 = р2 /T2 (рис. 4.2).
3. Изобарный процесс. Это обратимый процесс, протекающий при постоянном давлении р = р0 = const. Для него уравнение pV = νRT примет вид:
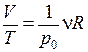 = const.
= const.
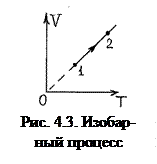
Это уравнение изобары. На изобаре V1 /T1 = V2 /T2 (рис. 4/3).
4. Адиабатный процесс. Это обратимый процесс в газе, протекающий без теплообмена с окружающей средой, т. е. при котором Q = 0. Адиабатный процесс может быть проведён в цилиндре с теплонепроницаемыми стенками, если поршень медленно поднимать или опускать (рис. 4.4). При этом энергообмен с окружающей средой происходит только в форме механической работы.
 Получим уравнение адиабатного процесса аналогично трём первым. Для этого запишем первый закон термодинамики:
Получим уравнение адиабатного процесса аналогично трём первым. Для этого запишем первый закон термодинамики:
dQ = pdV + νCV dT.
Так как у нас dQ = 0, то
νCV d T= −pdV.
Подставляя сюда р = νRT/V, получим:
CV dT = − 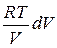 , или
, или 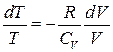 .
.
Интегрирование даёт:
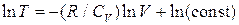 ,
,
или:
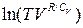 = ln(const),
= ln(const),
или:
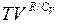 = const.
= const.
А так как R = Cp − CV, то, обозначая
Ср /СV = γ,
получаем:
TV(γ−1) = const. (4.2)
Это и есть уравнение адиабаты в координатах (V, Т).
Замечание 1. Величина
γ = Ср /СV
называется показателем адиабаты.
Для получения уравнения адиабаты в координатах (р, V) подставим в (4.2) T = pV/(νR) из уравнения состояния. Это даёт:
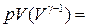 const,
const,
или:
pV γ = соnst. (4.3)
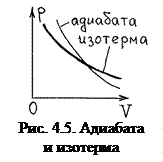
Замечание 2. Уравнение (4.3) похоже на уравнение изотермы (4.1), только у адиабаты график р(V) идёт круче, так как γ = Ср /СV > 1 (рис. 4.5).
И, наконец, получим уравнение адиабаты в координатах (р, Т). Для этого подставим в (4.2) V = νRT/p из уравнения состояния. Это даёт:
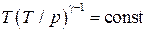 ,
,
или:
Т γ р1−γ = const,
или:
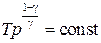 . (4.4)
. (4.4)
Замечание 3. Так как СV = 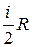 , Ср = СV + R =
, Ср = СV + R = 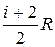 , то
, то
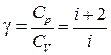 .
.
Для одноатомных газов (i = 3) γ = 5/3,
для двухатомных газов (i = 5) γ = 7/5 = 1,4,
для многоатомных газов (i = 6) γ = 4/3.
| <== предыдущая лекция | | | следующая лекция ==> |
| Теплоёмкости идеального газа | | | Общий подход к уравнению Шредингера в случае слабого потенциала |
Дата добавления: 2020-05-20; просмотров: 282;










