Приближение независимых частиц
Рассмотрим, как можно найти максимально близкие к точным волновые функции и уровни энергии неподвижного N-электронного атома, выбрав начало координат на его ядре с зарядом Z¦e¦. Гамильтониан в этом случае имеет вид:

Вначале рассмотрим, что будет, если просто исключить из (1.20) оператор энергии межэлектронного взаимодействия Vээ. Многоэлектронное уравнение Шредингера в этом случае распадается на систему из N одноэлектронных уравнений

c одноэлектронными гамильтонианами

Согласно (1.21), электрон iописывается волновой функцией 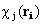 и имеет энергию e j. Это означает, что поведение каждого электрона не зависит от поведения остальных электронов и описывается некоторой волновой функцией, подобно единственному электрону в атоме водорода. В этом состоит суть приближения независимых частиц. Решения одноэлектронных уравнений (1.21)
и имеет энергию e j. Это означает, что поведение каждого электрона не зависит от поведения остальных электронов и описывается некоторой волновой функцией, подобно единственному электрону в атоме водорода. В этом состоит суть приближения независимых частиц. Решения одноэлектронных уравнений (1.21) 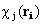 называются одноэлектронными волновыми функциями или орбиталями (в атоме - атомными орбиталями, в молекуле – молекулярными, в кристалле - кристаллическими).
называются одноэлектронными волновыми функциями или орбиталями (в атоме - атомными орбиталями, в молекуле – молекулярными, в кристалле - кристаллическими).
Полный гамильтониан атома, в этом приближении, есть просто сумма одноэлектронных гамильтонианов:

его собственные функции представляют собой произведение заселенных электронами атомных орбиталей

а энергия атома является суммой индивидуальных орбитальных энергий:

Приближенная волновая функция вида (1.24) называется волновой функцией Хартри.
Гамильтониан (1.22) является, конечно, чрезмерно упрощенным: электрон-электронное отталкивание не мало и пренебрегать им нельзя.
Дата добавления: 2022-04-12; просмотров: 122;










