Принципы квантовой механики
Основой для изучения квантовой химии являются курсы “Теоретические основы химии”, "Высшая математика" и "Физика", которые изучаются в РХТУ в 1-4 семестрах. Напомним, что квантовая химия атомов, молекул и их ансамблей и кристаллов опирается на следующие основные постулаты квантовой механики:
1.Каждое состояние системы n частиц полностью описывается функцией координат частиц x и времени t Y ({x},t), называемой волновой функцией. Волновая функция существует во всем интервале изменения переменных, где она непрерывна, конечна и однозначна. Выражение  имеет смыслвероятности того, что в момент времени t i-ая частица находится в интервале координат от xi до xi+dxi , а интеграл
имеет смыслвероятности того, что в момент времени t i-ая частица находится в интервале координат от xi до xi+dxi , а интеграл 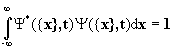 , при условии, что волновые функции нормированы на единицу. Поскольку физический смысл имеет лишь величина Y*Y, то волновая функция определена с точностью до произвольного фазового множителя типа eia .
, при условии, что волновые функции нормированы на единицу. Поскольку физический смысл имеет лишь величина Y*Y, то волновая функция определена с точностью до произвольного фазового множителя типа eia .
2.Каждой доступной измерению величине А в любом из возможных состояний соответствует линейный эрмитов операторА.Оператором называется символ, обозначающий математическую операцию, с помощью которой из одной функции получается другая; каждому оператору отвечает уравнение типа Аf=af, где а - вообще говоря комплексное число, называемое собственным значением оператора А, а f называется собственной функцией А. Оператор, обладающий свойством
 ,
,
называется эрмитовым; собственные значения эрмитовых операторов - действительные числа, а их собственные функции образуют полную ортонормированную систему, т.е. 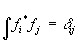 . Действуя на волновую функцию, оператор превращает ее в другую волновую функцию; говорят, что действие оператора переводит систему в другое состояние (частный случай - система остается в том же состоянии).
. Действуя на волновую функцию, оператор превращает ее в другую волновую функцию; говорят, что действие оператора переводит систему в другое состояние (частный случай - система остается в том же состоянии).
Таблица 1.1. Операторы основных физических величин
| Переменная | Обозначение переменной | Обозначение оператора | Производимая операция |
| Координата | r | r | Умножение на r |
| Момент | p | p | 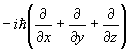
|
| Кинетическая Энергия | T | T |  
|
| Потенциальная энергия | V(r) | V(r) | Умножение на V(r) |
| Полная энергия | E | H | 
|
3. Независящая от времени волновая функция удовлетворяет стационарному уравнению Шредингера:
HY= ЕY (1.1).
Здесь H=T+V- эрмитов оператор полной энергии системы (гамильтониан) есть сумма оператора кинетической энергии всех частиц системыТ и оператора их потенциальной энергии V,Е - полная энергия системы. Квантовая химия изучает свойства атомов, молекул и кристаллов, состоящих из положительных ядер и отрицательных электронов, потенциальная энергия которых определяется кулоновским взаимодействием. Операторы кинетической энергии в системе М ядер и N электронов выглядят так:

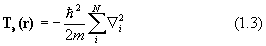
Здесь Ma – масса ядра a; m - масса электрона;
 - оператор Лапласа (лапласиан).
- оператор Лапласа (лапласиан).
Дифференцирование в уравнении (1.2) ведется по координатам ядер, в (1.3) – по координатам электронов.
Вид операторов потенциальной энергии (в системе СИ) следующий:



где Za и Zb - атомный номер элемента, e - заряд электрона, Rab – расстояние между ядрами, rij – расстояние между электронами.
Оператор (1.4) описывает отталкивание ядер, (1,5)– энергию притяжения электронов к ядрам, (1.6) – отталкивание электронов.
Строго говоря, в гамильтониане следует учесть релятивистские эффекты, обусловленые близкой к световой скоростью электронов в низкоэнергетических состояниях (электронов остова), спин-орбитальным взаимодействием и взаимодействием Дарвина, возникающим вследствие малых флуктуаций движущихся электронов относительно средних позиций. Однако, в очень хорошем приближении их можно игнорировать при рассмотрении многих квантовохимических задач, за исключением тяжелых (Z > 18) атомов и их ансамблей.
Зависящая от времени волновая функция удовлетворяет нестационарному уравнению Шредингера  .
.
4. Значения величины А, которые могут быть измерены, являются собственными значениями аi уравнения на собственные значения
АYi = аiYi , (1.7а)

где собственная функция Y i есть волновая функция, описывающая возможные состояния системы, в которых проводятся измерения. Это означает, что решение уравнения Шредингера (1.1) есть не что иное как решение задачи на собственные значения оператора полной энергии системы Н. Спектр собственных значений и набор собственных функций гамильтониана полностью характеризуют систему.
5. Среднее значение <а> величины А для системы, находящейся в состоянии i, определяется выражением: 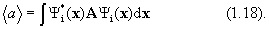
(предполагается, что волновые функции  ортонормальны). Это дает рецепт определения характеристик системы с помощью волновых функциий.
ортонормальны). Это дает рецепт определения характеристик системы с помощью волновых функциий.
Дата добавления: 2022-04-12; просмотров: 94;










