Факторы, влияющие на полноту осаждения
В природе нет абсолютно нерастворимых веществ. Поэтому осаждение не может быть совершенно полным. Необходимо было ввести какой-то единый критерий полноты осаждения. Договорились условием практически полного осаждения считать концентрацию осаждаемых ионов в растворе над осадком 1·10-6моль/л.
Рассмотрим факторы, влияющие на полноту осаждения.
1. Растворимость осаждаемого соединения.
При прочих равных условиях всякое отделение будет тем более полным, чем менее растворимо то соединение, в виде которого осаждается данный ион.
2. Количество осадителя.
Добавление избытка осадителя повышает полноту осаждения (действие одноименного иона). Для достижения полного осаждения определяемых ионов к исследуемому раствору прибавляют избыток осадителя. Однако при очень большом избытке осадителя может наступить обратное явление вследствие солевого эффекта или протекания реакций комплексообразования ионов осадка с ионами осадителя. Например:
Bi3+ + I– ó BiI3↓
BiI3↓ + I– ó [BiI4]–
HgI2↓ + 2I– ó [HgI4]2–
AgCl↓ + HCl ó HAgCl2
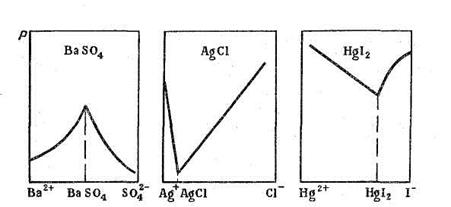
Таким образом, избыток осадителя не всегда способствует более полному осаждению. В ряде случаев растворимость осадка увеличивается, как это показано на рис. 6.1.
|
Рис. 6.1. Зависимость растворимости осадков от избытка осадителя
В аналитической практике обычно используют избыток осадителя 50% от его эквивалентного количества, т.е. полуторакратный избыток осадителя.
3. Степень ионизации электролита-осадителя.
Например, осаждение Mg2+ происходит более полно, если в качестве осадителя используют раствор NaOH, а не NH3·H2O. Концентрация OH- – ионов в первом растворе в 100 раз больше, чем во втором (степень диссоциации гидроксида натрия 100%, а гидроксида аммония – около 1%).
4. Влияние рН.
Практически полное осаждение сульфидов происходит при определенном значении рН. Причем для сульфидов катионов IV группы это рН=0,5, а для сульфидов катионов ІІІ группы – 9,25, что обусловлено их растворимостью. Выведем условие практически полного осаждения сульфидов двухвалентных металлов.
Me2+ + S2- ó MeS↓
Осадок выпадает, когда [Me2+]·[S2-] ≥ ПРMeS
Как осадитель используют сероводородную кислоту. В растворе она диссоциирует ступенчато:
H2S ó H+ + HS–
HS– ó H+ + S2–
Kобщ = К1·К2 = 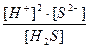
Отсюда концентрацию ионов водорода можно выразить
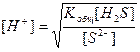
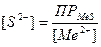
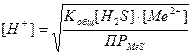
Концентрация сероводорода в насыщенном растворе 0,1 моль/л, тогда [H2S] ≈ 0,1моль/л; [Me2+] = 10-6моль/л (условие практически полного осаждения). Подставив числовые значения, получаем:
[H+] = 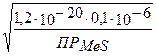
pH = 13,5 + 1/2·lgПРMeS
Дата добавления: 2017-03-12; просмотров: 8934;