Определение и строение молекул алкенов
Алкены –органические соединения, углеводороды алифатического (ациклического) непредельного характера, в молекуле которых между атомами углерода – одна двойная связь, и которые соответствуют общей формуле CnH2n.
Свое второе название -олефины - алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров - масел.
Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов − алканов.
Простейший алкен: C2H4 или H – C = C – H этен или этилен,
| |
H H
А его радикал: C2H3- или CH2=CH- − винил.
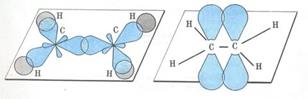
Атомы углерода, между которыми есть двойная связь, 'находятся в состоянии sр2−гибридизации. Это означает, что в гибридизации участвуют одна s- и две р-орбитали, а одна р-орбиталь остается негибридизованной. Перекрывание гибридных орбиталей приводит к образованию σ-связи, а за счет негибридизованных р-орбиталей соседних атомов углерода образуется вторая, π-связь. Таким образом, двойная связь состоит из одной σ- и одной π-связи.


 |
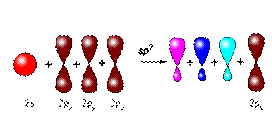 |
 |
σ
 |
-связь π-связь
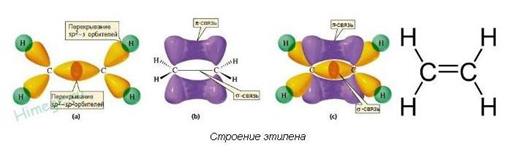 |
Три гибридные орбитали атома углерода, образующих двойную связь, одинаковы по форме и энергии, находятся в одной плоскости и направлены в углы равностороннего треугольника. Углы между гибридными орбиталями равны 120°. Негибридные орбитали, образующие π-связь, располагаются перпендикулярно плоскости молекулы.
Длина двойной связи 0,134нм (она короче одинарной, длина которой 0,154 нм), она более прочная, чем одинарная, так как ее энергия больше. Тем не менее, в углеродных соединениях π-связь значительно слабее, чем σ-связь и под воздействием реагентов π-связь легко разрывается. Наличие подвижной, легко поляризуемой π-связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.
Дата добавления: 2017-03-12; просмотров: 1275;