Подставим уравнение (9) в (7), для каждого реагента и упростим
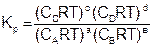
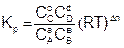 , (10)
, (10)
где Dn – изменение числа молей газообразных участников реакции
Dn = (с + d) – (а + в) (11)
Следовательно,
KР = КС(RT)Δn (12)
Из уравнения (12) видно, что KР = КС, если не меняется количество молей газообразных участников реакции (Δn = 0) или газы в системе отсутствуют.
Необходимо отметить, что в случае гетерогенного процесса концентрацию твердой или жидкой фазы в системе не учитывают.
Например, константа равновесия для реакции вида 2А + 3В = С + 4D, при условии, что все вещества газы и имеет вид
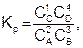 (13)
(13)
а если D – твердое, то
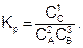 (14)
(14)
Константа равновесия имеет большое теоретическое и практическое значение. Численное значение константы равновесия позволяет судить о практической возможности и глубине протекания химической реакции.
Если K > 1,то данная реакция протекает со значительным выходом продуктов реакции; если K > 104, то реакция необратима; если K < 1, то такая реакция нетехнологична; если K < 10-4, то такая реакция невозможна.
Зная константу равновесия, можно определить состав реакционной смеси в момент равновесия и рассчитать константу выхода продуктов реакции. Константу равновесия можно определить, используя экспериментальные методы, анализируя количественный состав реакционной смеси в момент равновесия, или применяя теоретические расчеты. Для многих реакций при стандартных условиях константа равновесия – это табличная величина.
Дата добавления: 2021-02-19; просмотров: 134;