ЭЛЕКТРОЛИТЫ И НЕЭЛЕКТРОЛИТЫ
Вещества, растворы и расплавы которых проводят электрический ток в растворах или расплавах, называют электролитами. Мы будем говорить только о веществах - электролитах, подразумевая их нахождение в растворах.
Вещества
 |  | ||
Электролиты Неэлектролиты
растворы солей, кислот сахар, бензин, бензол, хлороформ
оснований глицерин спирт, газы.
К ним относятся вещества с ионной и полярной ковалентной связью (KCl, NiSO4, HCl, H2SO4 , NaOH, Ba(OH)2 , KOH и др.). Сами электролиты еще делятся на сильные, слабые, средние электролиты. Особенно важна такая классификация для кислот. Если отнесение солей и оснований к сильным электролитам можно приблизительно сделать по растворимости, то для кислот необходимо рассмотрение многих факторов по составу, строению. Классификация электролитов по силе приведена таблице (приложение 1).
Сухие соли и основания, безводные кислоты электрический ток не проводят. Это говорит о том, что при растворении в воде такие вещества претерпевают серьезные изменения. Электропроводность растворов этих веществ объясняет теория электролитической диссоциации (ТЭД), начала которой положил Сванте Август Аррениус в 1887 году.
II. ДИССОЦИАЦИЯ ЭЛЕКТРОЛИТОВ. ОКРАСКА ИНДИКАТОРОВ В РАЗЛИЧНЫХ СРЕДАХ
Процесс распада веществ электролитов на ионы пол действием растворителя или в расплаве называется электролитической диссоциацией.
Это обратимый процесс и обозначается стрелочками обратимости *:
ионизация
 Na Cl Na+ + Cl-
Na Cl Na+ + Cl-

моляризация
Сколько молекул распадается на ионы, столько молекул и образуется.
* некоторые авторы процессы диссоциации сильных электролитов изображают стрелкой, направленной вперед, а слабых электролитов - обратимыми стредками. Однако, это только символ в помощь для графического различия процессов у разных по природе веществ.
Основные положения ТЭД
1. Электролиты при растворении в воде диссоциируют на ионы: катионы и анионы. Количество катионов и анионов может быть различным, но суммарный заряд всех катионов всегда равен суммарному заряду всех анионов, поэтому, весь раствор в целом остается электрически нейтральным.
Ионы – это атомы или группы атомов, имеющие положительный или отрицательный заряд.
Простые ионы: Сl-, F-, S2-, Na+, Mg2+ и др.
Сложные ионы: PO43-, NH4+, SO42- и др.
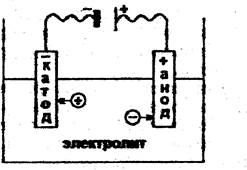
2. При пропускании электрического тока через раствор электролита ионы приобретают направленное движение: катионы движутся к отрицательно заряженному катоду, а анионы к положительно заряженному аноду.
 В обычных условиях ионы (без тока) совершают беспорядочное движение:
В обычных условиях ионы (без тока) совершают беспорядочное движение:
 К(-) А (+)
К(-) А (+)





 + __ + + + + + __
+ __ + + + + + __




 __ + __ __ + + __ __
__ + __ __ + + __ __
 __
__
 |




 . + __ + + __ __
. + __ + + __ __
а) б)
в)
Рис. 1. Хаотическое движение ионов (электрический ток
отсутствует) а); направленное движение ионов в растворе
электролита под действием электрического тока б), в).
3. Диссоциация – это обратимый процесс, поэтому с течением времени наступает химическое равновесие. При этом число молекул распавшихся на ионы (диссоциация) равно числу вновь образовавшихся из ионов.
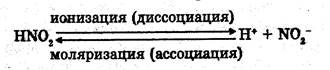
Свойства ионов отличаются от свойств соответствующих атомов, так как строение их различно, например атом хлора (простое вещество – хлор Сl2) и ион Сl- (хлорид-анион):
+17 Сl ) ) ) +17 Сl - ) ) )
2 8 7 2 8 8
Хлор – газ, молекула которого состоит из двух атомов хлора ядовит, сильный окислитель, анион хлора входит в состав поваренной соли, поступает в организм с пищей, не ядовит, в реакциях может быть только восстановителем.
Механизм диссоциации
В основе механизма диссоциации лежит гидратная теория растворов Д.И.Менделеева, развитая И.А.Каблуковым. Основную роль при диссоциации электролитов в растворах воды играет полярное строение молекул воды:
 О _
О _

 Н Н + диполь
Н Н + диполь
При растворении вещества с ионной связью в воде полярные молекулы воды ориентируются вокруг ионов вещества:
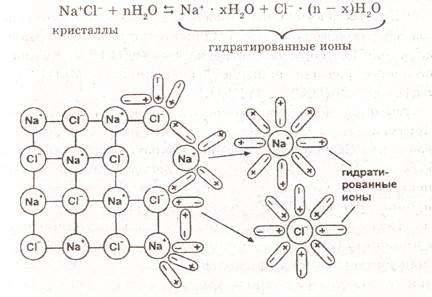
Рис. 2. Схема электролитической диссоциации электролита
с ионной связью (хлорида натрия) в водном растворе.
Возникают силы взаимодействия между ионами веществ и молекуляами воды.В результате ослабевает притяжение между ионами в электролите в 81 раз (для растворителя – воды). Электролит распадается на гидратированные ионы, то есть, окруженные молекулами воды.
При диссоциации кислот происходит не просто распад на ионы, а каждый катион водорода удерживает молекулу воды и образуется гидрат постоянного состава. Такой гидратированный протон изображают:
Н+ + Н2О = Н3О+
ион гидроксония
Процесс электролитической диссоциации хлороводорода (вещество с полярной ковалентной связью) с учетом гидратации можно представить так:
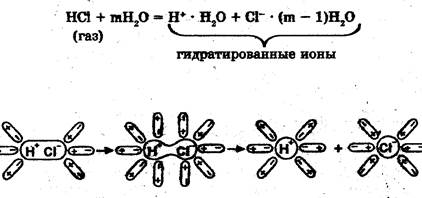
Рис. 3. Схема электролитической диссоциации электролита с полярной
ковалентной связью (хлороводорода) в водном растворе.
При растворении в воде происходит ориентация диполей воды и возникают междипольные связи. В результате диполь-дипольного взаимодействия изменяется характер химической связи в молекуле НCl. Связь «дополяризуется» и затем становится ионной. Она легко разрывается с образованием гидратированных ионов.
В образовании гидратированных ионов большую роль играют донорно-акцепторныое, диполь-дипольное и ион-дипольное взамодействия, водородные связи.
Роль донорно-акцепторного взаимодействия (см. раздел 5) в образовании, например, иона H3О+ можно показать следующей схемой:
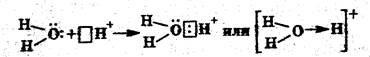
Диссоциация кислот
Кислотами называются электролиты, которые в водных растворах диссоциируют с образованием только одного вида катионов – катионов водорода.
HNO3 ßà H+ + NO3 - (нитрат-анион)
HCl ßà H+ + Cl- (хлорид-анион)
Многоосновные кислоты диссоциируют ступенчато:
H2SO4 ßà H+ + HSO4- (гидросульфат-ион)
HSO4- ßà H+ + SO42- (сульфат-анион)
Легче диссоциация протекает по 1-ой ступени, по 2- ой и 3-ей ступени диссоциация протекает очень трудно, так как положительная частица отрывается от отрицательно-заряженной частицы, которая хорошо притягивает катион водорода:
H 3PO4 ßà H+ + H2 РO4 - (дигидрофосфат-анион)
H 2 РO4 - ß à H+ + H РO4 2- (гидрофосфат-анион)
H РO4 2- ßà H+ + РO4 3- (фосфат-анион)
Диссоциация оснований
Основания – Это электролиты, которые в водных растворах диссоциируют с образованием только одного вида анионов - гидроксид - анионов. Их принято называть гидроксидами, хотя кислородосодержащие кислоты тоже относятся к гидроксидам (кислотным).
NaOH ßà Na+ + OH—
Многокислотные основания диссоциируют ступенчато:
Са(ОН)2 ßà СаОН+ + ОН-
СаOH+ ßà Ca2+ + OH-
катион гидроксокальция
или гидроксокатион кальция
Диссоциация амфотерных гидроксидов
Диссоциируют очень слабо двояко: и как основания и как кислоты
а) в кислой среде, как основания:
Zn(ОН)2 ßà Zn2+ + 2ОН- (суммарно)
или:
Zn(ОН)2 ßà ZnОН+ + ОН-
ZnOH + ßà Zn2+ + OH-
катион гидроксоцинка
или гидроксокатион цинка
б) в щелочной среде: Zn(ОН)2 ß à2H+ + ZnO 22- (суммарно)
или
Zn(OH)2 ß à H+ + HZnO2— гидроксоцинкат-анион
HZnO2— ßà H+ + ZnO22- цинкат-анион
Диссоциация солей
Средние соли – это электролиты, которые в водных растворах диссоциируют на катионы металла (или аммония) и кислотный остаток.
CaCl2 ßà Ca2+ + Cl-
хлорид кальция
Na2SO4 ßà 2Na+ + SO42—
сульфат натрия
Кислые соли – диссоциируют на катионы металла и кислотный остаток, содержащий в своем составе водород.
В небольшой степени этот водород также отщепляется в виде катиона.
NaHCO3 ßà Na+ + HCO3—
гидрокарбонат натрия
Основные соли – диссоциируют на кислотный остаток и катион, содержащий гидроксо-группу.
CaOHCl ßà CaOH+ + Cl-
гидроксохлорид кальция
(ZnOH)2SO4 ßà 2 ZnOH+ + SO42-
гидроксосульфат цинка
В небольшой степени гидроксо-группа также отщепляется в виде аниона.
Таким образом, наличие катиона водорода (Н+) или гидроксид-аниона
(ОН-) отвечает, соответственно, за кислую и щелочную среду растворов и окраску индикаторов.
Окраска индикаторов
| Название индикатора | Кислая среда | Нейтральная среда | Щелочная среда |
| Универсальный | Красный | Желтый | Синий |
| Лакмус | Красный | Фиолетовый | Синий |
| Синий лакмус | Красный (изменяет окраску) | Синий (не изменяет окраску) | Синий (не изменяет окраску) |
| Красный лакмус | Красный (не изменяет окраску) | Красный (не изменяет окраску) | Синий (из меняет окраску) |
| Метиловый красный | Красный | Красный | Желтый |
| Метиловый оранжевый | Розовый (красный) | Оранжевый (желтый) | Желтый |
| Фенолфталеиновый | Бесцветный | Бесцветный | Малиновый |
| Тимоловый фталеиновый | Бесцветный | Бесцветный | Синий |
III. СТЕПЕНЬ ДИССОЦИАЦИИ. КОНСТАНТА ДИССОЦИАЦИИ.
Количественными характеристиками силы электролитов являются степень диссоциации и константа диссоциации.
Степень диссоциация
Степень диссоциации - это отношение числа молекул, распавшихся на ионы к общему числу растворенных молекул электролита. Выражается в долях и в процентах.
с1
 a = ∙ 100 %
a = ∙ 100 %
с
a – степень диссоциации
с1 – концентрация молекул электролита, распавшегося на ионы;
с – общая концентрация молекул электролита.
Например, из 0,05 моль H2SO3, растворенных в воде, на ионы распалось 0,01 моль. Найти степень диссоциации H2SO3.
0,01
 a = ∙ 100% = 20 %
a = ∙ 100% = 20 %
0,05
Это означает, что из 100 молекул сернистой кислоты на ионы распалось только 20.
Степень диссоциации зависит:
1) от природы растворителя; например, СоCl2 – синего цвета, а гидратированные ионы Со2+ - розового цвета. Если хлорид кобальта растворить в воде, то раствор становится розовым, образуется много ионов. Большинство молекул распались на ионы. Если растворить эту же соль в спирте, то раствор имеет синий цвет, т.к. в растворе в основном находятся молекулы. При растворении в воде сила притяжения в между ионами Со2+ и Сl- ослабевает в 81 раз по сравнению с вакуумом, а в спирте, - только в 27,8 раз. Поэтому в воде больше молекул распадаются на ионы. Таким образом, чем больше диэлектриическая проницаемость - ε (величина постоянная) растворителя, тем больше степень диссоциации электролита в нем;
2) от концентрации (разбавления раствора)
разб. р-р
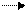
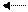 СuСl2 Cu2+ + 2Cl—
СuСl2 Cu2+ + 2Cl—
зеленый конц. р-р голубой р-р
При разбавлении равновесие сместилось вправо, т.к. при разбавлении увеличилось число катионов, а гидратированные катионы меди (+2) окрашены в голубой цвет.
Таким образом, чем больше концентрация, тем меньше степень диссоциации, а чем меньше концентрация, тем больше степень диссоциации.
3) от природы электролита: цинк реагирует с равными объемами кислот одинаковой концентрации, а реакция идет с разными скоростями:
Zn + 2 HCl = ZnCl2 + H2↑
соляная кислота
(сильная)
Zn + 2CН3COOH = (CH3COO)2 Zn + H2 ↑
уксусная кислота
(слабая)
Реакция с соляной кислотой протекает бурно и быстрее, чем с уксусной
кислотой, так как последняя образует меньще ионов при диссоциации, чем
соляная кислота.
4) от добавления к раствору первого электролита электролита № 2 с одноименным ионом первому электролиту; степень диссоциации 1-го электролита уменьшается.
Опыт:
В пробирку нальем 1 мл раствора воды и добавим по 2 капли растворов NH4OH и фенолфталеина. Раствор окрасится в малиновый цвет (среда щелочная).
Затем добавим электролит с одноименным ионом NH4Cl – хлорид аммония (содержит катион аммония NH4+), при этом раствор обесцвечивается:
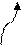 NH4OH ßà NH4+ + OH—
NH4OH ßà NH4+ + OH—
 создает щелочную среду
создает щелочную среду
NH4Clßà NH4+ + Cl—
C увеличением числа одноименных ионов NH4+ при добавлении хлорида аммония равновесие смещается влево ( по принципу Ле Шателье), так как катионы аммония связывают почти все гидроксид-ионы в молекулы NH4OH и ранее малиновый раствор обесцвечивается;
5) от температуры: при ее повышении степень диссоциации увеличивается для слабых электролитов (эндотермическая реакция);
6) от числа атомов кислорода в молекуле кислородосодержащих кислот: чем больше атомов кислорода в молекуле кислот, тем больше степень ее диссоциации;
например HСlO -хлорноватистая кислота практически не распадается
на ионы, она слабее угольной(<0,17 %);
сравните:
• HСlO3 (хлорноватая) a =90 %
• HClO4 (Хлорная) a = 95 %
7) от радиуса аниона (поляризуемости) в безкислородных кислотах:
сила кислот увеличивается в ряду: HF HCl HBr HI;
связь Н – Гал ослабевает, так как радиус и поляризуемость йодид- аниона увеличиваются.
По силе электролиты делят на:
А) сильные (d> 30%); к ним относят
• все растворы солей кроме роданида железа(Ш), хлорида
ртути(П), хлората ртути (П);
• кислоты: соляная – 98%; серная – 58%; азотная – 91%;
бромоводородная – 92%;
• основания: КОН –84%; NaОН - 84%; Ва(ОН)2 – 92 %;
Б) средней силы ( a= 2-30%):
• фосфорная кислота –26%; азотистая кислота– 6,5%; H2F2 –8.5%
В) слабые (a < 2 5): уксусная кислота – 1,3 %; гидроксид аммония –
1,3 %; угольная кислота –0,17 %; сероводородная –0,07 %;
HCN- 0,01% ; к ним относятся также основания не щелочных и не щелочноземельных металлов, примеры приведены в таблице (приложение 1).
Константа диссоциации
Процесс диссоциации обратимый, и с течением времени устанавливается
химическое равновесие:
CH3COOH ßà H+ + CH3COO—
уксусная кислота ацетат-анион
Применив к нему закон действующих (действия) масс*, получим:
[H+] [CH3COO-]
 K дисс. = = 1,86 . 10—5
K дисс. = = 1,86 . 10—5
[ CH3COOH]
*Закон действующих масс для слабых электролитов и газов в реакциях
говорит о том, что скорость реакции прямопропорциональна произведению равновесных концентраций веществ, взятых в степенях, равных их стехиометрическим коэффициентам.
Например,
аA + bB ßà d D + fF
В момент равновесия скорости прямой и обратной реакций будут равны:
V прямой реакции = V обратной реакции
→ ←
k ∙[A] a∙ [B] b = k ∙ [D] d ∙ [F] f
Тогда из математической пропорции можно записать:
→
k [D] d ∙ [F] f

 = = K равновесия
= = K равновесия
←
k [A] a∙ [B] b
K равновесия - константа равновесия. В случае диссоциации электролитов она называется константой диссоциации электролита (К.Д.Э.)
К.Д.Э. – это отношение произведения концентрации ионов к концентрации недиссоциированных молекул слабого электролита, взятых в степенях, равных стехиометрическим коэффициентам в уравнении диссоциации.
По ее величине можно судить о силе электролита. Чем больше константа диссоциации, тем больше концентрация ионов и сильнее электролит.
Константа диссоциации зависит от тех же факторов, что и степень диссоциации.
IV. ДИССОЦИАЦИЯ ВОДЫ. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ. ВЕЛИЧИНА рН (ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ).
Вода - очень слабый электролит и диссоциирует на ионы в незначительной степени:
2Н2О ßà H3O+3 + OH- или
НОН ßà H+ + OH—
[H+] ∙ [ OH--]
 K дисс = = 1,8 • 10—16
K дисс = = 1,8 • 10—16
[ HOH]
Константа равновесия или диссоциации воды очень незначительна, тогда концентрацию недиссоциированных молекул воды можно принять за величину постоянную и равную для объема воды равного одному литру (1 л):
m (H2O) 1000г

 [HOH] = = = 55,5 моль\л
[HOH] = = = 55,5 моль\л
M (HOH) 18 г/моль
Это значение велико по сравнению с Кдисс.
Домножим левую и правую часть выражения для константы диссоциации на [HOH], тогда произведение Кдисс.∙ [HOH] = [H+]∙ [OH-] = 1,8 • 10—16 ∙ 55,5= 10—14
Кдисс.∙ [HOH] - ионное произведение воды - Кw
Кw = [H+] ∙ [OH-] = 10—14 - величина постоянная.
Отсюда следует: как бы не изменялась концентрация водородных и гидроксильных ионов в воде или в разбавленном водном растворе слабого электролита, их произведение всегда равно ионному произведению воды.
Так как [H+] = [OH-] в воде, то [H+] ∙ [OH-] = [ H+] 2 = [OH-] 2 = 10—14 ,

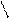
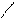
 тогда [H+] = [OH-] = Кw = 10—14 = 10—7 ,
тогда [H+] = [OH-] = Кw = 10—14 = 10—7 ,
Если к чистой воде добавить кислоты, то увеличится концентрация ионов Н+; допустим концентрация увеличилась от 10—7 до 10-4 , тогда
Кw 10-14

 [ OH-] = = = 10-10
[ OH-] = = = 10-10
[H+] 10—4
Если к чистой воде добавить щелочи. То увеличится концентрация ионов ОН- допустим от 10-7 до 10-3, тогда
Кw 10-14

 [ H+] = = = 10-11
[ H+] = = = 10-11
[ОH-] 10—3
Таким образом, в водных растворах с различной средой (кислотной, нейтральной, щелочной) всегда присутствуют ионы Н+ и ОН—
В нейтральной среде: [H+]=[OH-]= 10-7
В кислой среде: [H+] > 10-7 (например, 10-5, 10-3 , 10-1)
В щелочной среде: [H+] < 10-7 (например, 10-9, 10-11 , 10-13)
Концентрация ионов водорода выражается очень малыми величинами и пользоваться ими при расчете неудобно. Более удобная форма выражение концентраций через водородный показатель, который численно равен отрицательному логарифму концентрации водородных ионов:
рН = - lg [H+]
Отсюда рН = lg [H+] = -lg 10—7 = 7 (нейтральная среда)
рН = -lg 10—5 = 5 (кислая среда)
рН = -lg 10—10 = 10 (щелочная среда)
Для упрощенного расчета рН необходимо выполнить следующий алгоритм действий:
1) -пусть [Н+] = 10-6, тогда рН равен степени с противоположным
знаком, т.е. 6;
-пусть [Н+] = 10-4,7, тогда рН равен 4,7;
2) -пусть известна [OH-], тогда рН равен: 14 минус показатель степени
концентрации этих ионов; например, [ОН-] = 10-4,, тогда рН равен
14 – 4 = 10;
Шкала значений водородного показателя и концентрации катионов водорода
рН 1 2 3 4 5 6 7 8 9 10 11 12 13 14
[H+]10-1 10-2 10-3 10-4 10-5 10-6 10-7 10- 8 10-9 10-10 10-11 10-12 10-13 10-14


 сильно-кислая слабо-щелочная
сильно-кислая слабо-щелочная
слабо-кислая сильно-щелочная

 увеличение кислотности увеличение щелочности
увеличение кислотности увеличение щелочности
нейтральная
V. ПРОТОЛИТИЧЕСКАЯ ТЕОРИЯ БРЕНСТЕДА-ЛОУРИ
Протолитическая теория кислот и оснований, предложена в 1923 году датским ученым Бренстедом и английским ученым Лоури.
Согласно этой теории: кислотами (основаниями) являются вещества, молекулы или ионы, которые отдают (соотвественно, присоединяют) протоны. Как те, так и другие получили название протолитов. Под протоном понимают положительный ион водорода (катион водорода Н+).
Реакции отщепления протонов изображаются уравнением:
кислотаßà основание + Н+
Например:
HCl ßà + H+ + Cl-
где Сl- - основание, сопряженное кислоте HCl.
Свободные протоны в растворах самостоятельно не существуют. Они переходят от кислоты к какому-либо основанию, поэтому в растворе всегда протекают два процесса:
CH3COOH ßà CH3COO-- + H+
к-та 1 осн-ие 1
NH3 + H+ ßà NH4+
осн-ие 2 к-та 2
Равновесие между ними изображают:
кислота 1 + основание 2 ßà Основание 1 + кислота 2
 СH3COOH + :NH3 CH3COO- + NH4+
СH3COOH + :NH3 CH3COO- + NH4+
 | |||||
 | |||||
 | |||||
сопряженные кислота и сопряженные кислота и
основание №1 основание № 2
Таким образом, из кислоты и основания всегда получаются новые сопряженные кислота и основание. Теория расширила круг кислот и оснований – ими могут быть ионы. Одно и то же вещество в зависимости от того, с чем оно реагирует, может быть либо кислотой или основанием.
Льюис предложил общее определение:
кислота – это вещество, которое акцептирует электронную пару;
основание - это вещество, которое предоставляет электронную пару. Исходя из этого определения, взаимодействие между кислотами и основаниями сводится к формированию ковалентной связи по донорно-акцепторному механизму:
: NH3 + H+ à NH4+
Из представлений Бренстеда-Лоури вода обладает амфотерными свойствами, так как способна отдавать и присоединять протоны. В присутствии более сильных оснований вода ведет себя как кислота, а в присутствии более сильных кислот, как основание:
H2O + NH3 ßà NH4+ + OH—
к-та осн..
HCl + H2O ßà H3O+ + Cl-
к-та осн.
Теория вскрыла относительность понятий о кислотах и основаниях и показала, что продукты их взаимодействия следует рассматривать как новые кислоты и основания.
VI. РЕАКЦИИ ОБМЕНА В ВОДНЫХ РАСТВОРАХ ЭЛЕКТРОЛИТОВ. ИОННЫЕ РЕАКЦИИ И УРАВНЕНИЯ
Электролиты в водных растворах находятся в виде ионов или частично в виде ионов (сильные электролиты), а в основном в виде молекул (слабые электролиты). Реакции между водными растворами электролитов – это реакции, в которых участвуют ионы. Такие реакции называются ионными. Реакции такого типа возможны, если ионы одного вещества взаимодействуют с ионами другого вещества, связываются между собой и образуют:
А) нерастворимое вещество (осадок, в уравнении обозначают ↓)
Б) газообразное вещество (в уравнении обозначают ↑)
В) малодиссоциирующее вещество (слабый электролит, например, вода)
Г) комплексные соединения
Если в реакциях химические элементы не изменяют степени окисления, то реакции называются реакциями ионного обмена. Реакции будут необратимы и протекают до конца, если выполняются условия, обозначенные в пунктах а,б,в,г.
Случай 1. Реакция обмена с образованием осадка, например, между ортофосфорной кислотой и нитратом серебра:
Запишем уравнение реакции в молекулярной, полной ионной и сокращенной ионной форме:
1) молекулярная форма:
H3PO4 + 3AgNO3 à Ag3PO4 ¯ + 3НNO3
2) переписываем уравнение, изобразив хорошо диссоциирующие вещества в виде ионов, а уходящие из сферы реакции – в виде молекул:
3H+ + PO4 3- + 3Ag+ + 3NO3 -à Ag3PO4 ¯ + 3Н+ + 3NO3+
- это полное ионное уравнение;
3) исключаем из обеих частей равенства одинаковые ионы, т.е. ионы, не участвующие в образовании малодиссоциирующего вещества:
 |


 3H+ + PO4 3- + 3Ag+ + 3NO3 -à Ag3PO4 ¯ + 3Н+ + 3NO3-
3H+ + PO4 3- + 3Ag+ + 3NO3 -à Ag3PO4 ¯ + 3Н+ + 3NO3-
 |  |
4) выписываем оставшиеся ионы, участвующие в образовании малодиссоциирующего вещества:
3Ag+ + PO4 3- à Ag3PO4↓
- это сокращенное ионное уравнение
Случай 2. Реакция обмена с образованием газообразного вещества, например, между хлоридом аммония и известковой водой (гидроксидом кальция):
1) 2 NH4Cl + Ca(OH)2 à CaCl2 + 2 NH3↑ + 2 H2O
2) 2 NH4+ + 2 Cl - + Ca2+ + 2OH- à Ca2+ +2 Cl- + 2 NH3↑ + 2 H2O


 3) 2 NH4+ + 2 Cl - + Ca2+ + 2OH- à Ca2+ +2 Cl- + 2 NH3↑ + 2 H2O
3) 2 NH4+ + 2 Cl - + Ca2+ + 2OH- à Ca2+ +2 Cl- + 2 NH3↑ + 2 H2O
4) 2 NH4+ + 2OH- à 2 NH3↑ + 2 H2O
Случай 3. Реакция обмена с образованием воды (реакция нейтрализации):
1) NaOH + HCl à NaCl + H2O
2) Na+ + OH- + H+ + Cl- à Na+ + Cl- + H2O
 |  |  |  | ||||
3) Na+ + OH- + H+ + Cl- à Na+ + Cl- + H2O
4) H+ + OH- à H2O
Случай 4. Реакция с образованием комплексных ионов:
1) 2AgNO3 + 6NH3 +2 Н2O = 2[Ag(NH3)2]OH + 2NH 4NO3
Диамминсеребра (+1)
гидроксид
2) 2Ag++ 2NO3 - + 6NH3 +2 Н2O = 2[Ag(NH3)2]+ + 2OH- + 2NH4+ + 2 NO3 -
 3) 2Ag++ 2NO3 - + 6NH3 +2 Н2O = 2[Ag(NH3)2]+ + 2OH- + 2NH4+ + 2 NO3 -
3) 2Ag++ 2NO3 - + 6NH3 +2 Н2O = 2[Ag(NH3)2]+ + 2OH- + 2NH4+ + 2 NO3 -
4) 2Ag++ 6NH3 +2 Н2O = 2[Ag(NH3)2]+ + 2OH- + 2NH4+
При невыполнении таких условий реакции являются обратимыми и не протекают до конца, так как ионы не связываются и не выводятся из сферы реакции.
VII. ГИДРОЛИЗ СОЛЕЙ
Гидролиз соли – взаимодействие ионов соли и воды, приводящее к образованию слабого электролита.
Причина гидролиза – образование слабого электролита, следствие – в более частых случаях изменение рН среды.
«Hydro” – вода
«Lysis” – разложение.
Для того, чтобы определить подвергается соль гидролизу или нет необходимознатькакие основания и кислоты образуют данную соль в реакциях нейтрализации: сильные или слабые электролиты.
Типы гидролиза
1. Гидролиз по аниону(соль образована катионами сильных оснований и анионами слабых кислот);
2. Гидролиз по катиону(соль образована катионами слабых оснований и анионами сильных кислот);
3. Гидролиз смешанный – по катиону и аниону(соль образована катионами слабых оснований и анионами слабых кислот);
4. Соль гидролизу не подвергается, если образована катионами и анионами сильных электролитов.
Чтобы написать уравнения гидролиза, нужно рассмотреть из каких по силе электролитов (кислоты и щелочи) может быть получена данная соль, например,
сульфит бромид нитрит хлорид
натрия цинка аммония натрия

 Na2SO3 ZnBr2 NH4NO2 NaCl
Na2SO3 ZnBr2 NH4NO2 NaCl
 | |||||||||||
 |  | ||||||||||
 | |||||||||||
 | |||||||||||
 | |||||||||||
NaOH H2SO3; Zn(OH)2 HBr ; NH4OH HNO2 NaOH HCl
сильный слабый слабый сильный слабый слабый сильный сильный
(по аниону) (по катиону) (смешанный)
 подвергаются гидролизу не подвергается
подвергаются гидролизу не подвергается
Итак! Тип гидролиза определяется ионом слабого электролита, из которого получена соль.
Гидролиз в большинстве случаев процесс обратимый!
Гидролизможет протекатьв несколько ступеней,если для этого создать определенные условия усиления гидролиза. Число ступеней полного гидролиза определяется основностью или кислотностью слабых электролитов, которые образуют данную соль. Если соль подвергается смешанному гидролизу, то число ступеней определяется большей величиной этих показателей.
Например: для Na3РO4 – количество степеней гидролиза – 3, так как ортофосфорная кислота Н3РO4 – трехосновная;
для ZnBr2 - количество степеней гидролиза – 2, так как гидроксид цинка Zn(OH)2 - техкислотный гидроксид в основной форме;
для Cu(NO2) – нитрита меди (+2) количество ступеней -2, так как кислотность гидроксида меди (+2) равна двум, а основность азотистой кислоты меньше и равна одному.
Дата добавления: 2016-10-26; просмотров: 8758;










