Классификация химических реакций в органической и неорганической химии
Мир химических реакций огромен и многообразен. Сущность химических реакций состоит в превращении одних веществ в другие. При этом разрушается структура исходных веществ за счёт разрыва химических связей и возникают новые вещества с новыми связями и другим строением. Каждая химическая реакция имеет свои характеристики.
Неорганические реакции классифицируют по нескольким признакам. По числу и составу исходных веществ и продуктов реакции можно выделить следующие типы химических реакций: реакции соединения, реакции разложения, реакции замещения и реакции обмена.
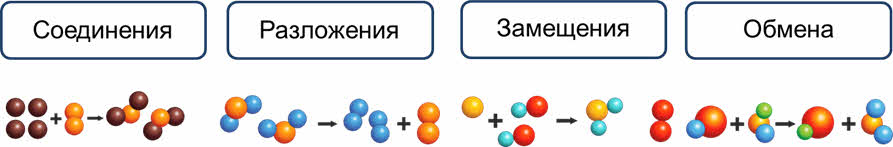
Реакции соединения – это реакции, в ходе которых из двух или более веществ образуется одно сложное вещество.
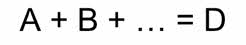
Существует большое число реакций соединения простых веществ: например, железа и хлора с образованием хлорида железа (III), водорода с хлором с образованием хлороводорода.
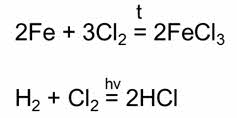
А также известно много реакций соединения сложных веществ: например, в результате взаимодействия оксида калия и воды образуется гидроксид калия, в реакции оксида магния и оксида серы (VI) образуется сульфат магния, в реакции хлорида железа (II) с хлором образуется хлорид железа (III).
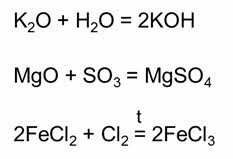
Реакциями разложения называются реакции, в результате которых из одного сложного вещества образуются два или более новых веществ.
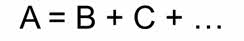
Так, в реакции разложения карбоната бария образуется оксид бария и углекислый газ, в реакции разложения нитрата серебра один образуется серебро, оксид азота (IV) и кислород, в реакции разложения малахита образуется оксид меди (II), углекислый газ и вода.
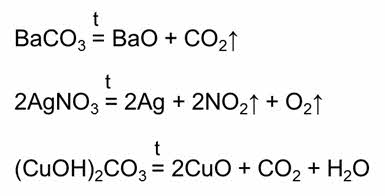
Реакции замещения – это реакции между простыми и сложными веществами, при протекании которых атомы простого вещества замещают атомы одного из элементов в молекуле сложного вещества.
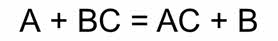
Например, в реакции алюминия с оксидом железа (III) образуется железо и оксид алюминия, в реакции хлора с бромидом калия образуется хлорид калия и бром, в реакции карбоната кальция с оксидом кремния (IV) образуется силикат кальция и углекислый газ.
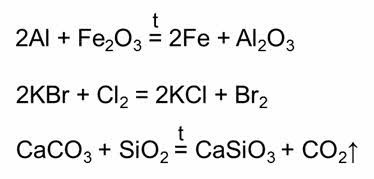
Реакциями обмена называются реакции между двумя сложными веществами, которые обмениваются своими составными частыми.
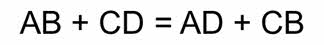
Так, в реакции азотной кислоты с гидроксидом натрия образуется нитрат натрия и вода, в реакции хлорида бария с серной кислотой образуется сульфат бария и соляная кислота, в реакции карбоната натрия с соляной кислотой образуется хлорид натрия, углекислый газ и вода.
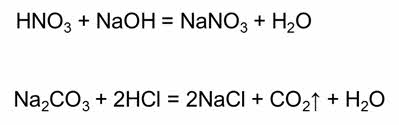
В результате реакций обмена обычно образуется осадок, газообразное вещество или слабый электролит.
По признаку изменения степеней окисления элементов в молекулах реагирующих веществ, все реакции делятся на: окислительно-восстановительные, которые идут с изменением степени окисления, и на реакции, идущие без изменения степени окисления.
Так, реакция разложения карбоната кальция до оксида кальция и оксида углерода (IV) не является окислительно-восстановительной, так как элементы здесь не изменяют свои степени окисления.
А реакция меди с хлором является окислительно-восстановительной, потому что медь повышает свою степень окисления с 0 до +2, а хлор понижает свою степень окисления с 0 до -1. Медь является восстановителем, а хлор – окислителем.

По знаку теплового эффекта все реакции делятся на: экзотермические, идущие с выделением теплоты, и эндотермические, которые идут с поглощением теплоты.
Например, реакция образования хлороводорода из водорода и хлора является экзотермической, а реакция образования оксида азота (II) из азота и кислорода является эндотермической.

По признаку однородности реакционной системы различают реакции гомогенные, протекающие в однородной системе, и гетерогенные, протекающие в неоднородной системе.
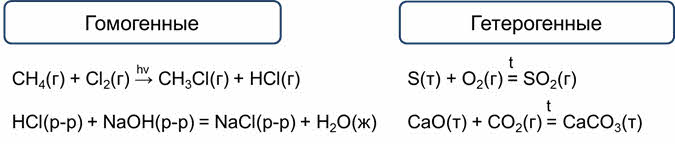
Например, реакция метана с хлором является гомогенной, потому что исходные вещества и продукт реакции находятся в одном агрегатном состоянии – газообразном.
Реакция соляной кислоты с гидроксидом натрия также является гомогенной, так как все вещества являются жидкостями.
А реакция серы с кислородом будет гетерогенной, так как сера является твёрдым веществом, а кислород и сернистый газ – газообразными.
Реакция оксида кальция с оксидом углерода (IV) также будет гетерогенной, потому что оксид кальция и карбонат кальция являются твёрдыми веществами, а оксид углерода (IV) – газом.
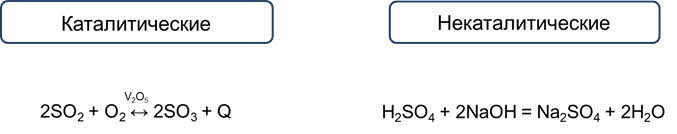
В зависимости от присутствия или отсутствия катализатора реакции делятся на: каталитические, которые идут с участием катализатора и некаталитические, идущие без участия катализатора.
Например, реакция образования оксида серы (VI) из оксида серы (IV) и кислорода является каталитической, так как эта реакция идёт в присутствии катализатора – оксида ванадия (V).
А реакция серной кислоты с гидроксидом натрия будет некаталитической, так как не требует участия катализатора.
По признаку обратимости все реакции делят на необратимые, которые идут только в одном направлении и на обратимые, которые идут одновременно в прямом и обратном направлении. Например, реакция образования аммиака из азота и водорода является обратимой, а реакция горения метана – необратимой.

В органической химии реакции классифицируют в зависимости от изменения строения реагирующих молекул и характера изменения связей. Кроме того, органические реакции имеют свои особенности.
Органические реакции идут медленно и требуют определённых условий: температура, давление, катализатор. Выход продуктов реакции невысокий, так как большинство реакций идёт в несколько стадий.

Cуществует несколько классификаций органических реакций.
Первая классификация по механизму реакции, то есть по разрыву ковалентной связи. Это гомолитические, или радикальные реакции, которые идут с образованием радикалов – частиц с неспаренным электроном. Их течение сопровождается гомолитическим разрывом связи.

Например, гомолотической реакцией является реакция хлорирования алканов, которая идёт по свободнорадикальному цепному механизму.
Гетэролитические, или ионные реакции протекают с образованием катиона и аниона. Гетэролитический разрыв ковалентной связи приводит к образованию нуклеофилов (анионов) и электрофилов (катионов).
В зависимости от природы атакующего реагента реакции могут быть нуклеофильными и электрофильными.
Нуклеофильными являются реакции, где реагентом является нуклеофил, то есть анион или молекула, которые предоставляют свою пару электронов на образование новой связи.
Например, в реакции хлорметана с с гидроксидом натрия гидроксид натрия выступает в роли нуклеофильного реагента.
Электрофильными называются реакии с электрофильными реагентами (электрофилами), то есть катионами или молекулами, которые имеют свободную орбиталь, которая может принять электроны для образования новой связи.
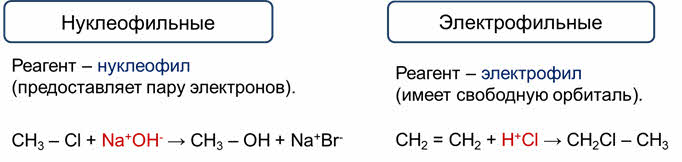
Так, в реакции этилена с хлороводородом электрофилом является катион водорода в составе хлороводорода.
В зависимости от изменения строения реагирующих веществ реакции разделяют на реакции замещения, присоединения, отщепления, разложения и изомеризации.
В реакциях замещения атом или группа атомов в исходной молекуле замещается на атом или группу атомов.
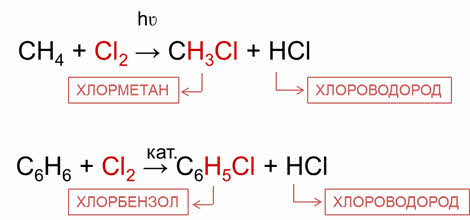
Например, в реакции хлорирования метана, атом хлора замещает один атом водорода в молекуле метана, при этом образуется хлорметан и хлороводород. В реакции бензола с хлором в присутствии катализатора, атом хлора также замещает один атом водорода в молекуле бензола и образуется бромбензол и хлороводород. Реакции замещения характерны для алканов, ароматических соединений, спиртов, фенолов, карбоновых кислот, углеводов.
В реакциях присоединения происходит разрыв пи-связей и присоединение к атомам углерода и гетероатомам фрагментов реагентов.
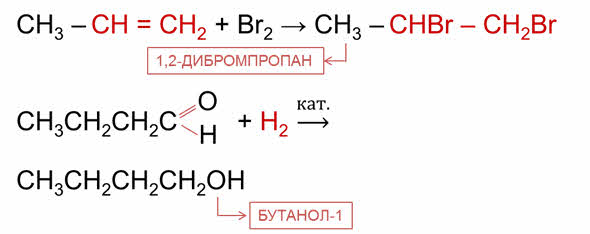
Например, в реакции пропена с бромом разрывается пи-связь в молекуле пропена и к каждому атому углерода при двойной связи присоединяется атом брома. В данной реакции образуется 1,2-дибромпропан. В реакции бутаналя с водородом в молекуле бутаналя также разрывается пи-связь, по месту разрыва этой связи присоединяется водород, при этом образуется бутанол-1.
Таким образом, реакции присоединения характерны для углеводородов с кратными связями, альдегидов, кетонов, моносахаридов, при определённых условиях эти реакции характерны и для ароматических соединений.
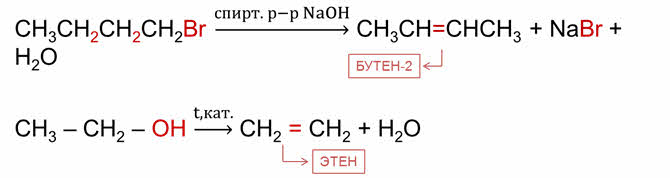
Реакции отщепления характерны для галогенуглеводородов и спиртов. Так, в реакции 1-бромбутана со спиртовым раствором щёлочи образуется бромид натрия, вода и бутен-2. При отщеплении воды от молекулы этанола образуется этен.
В ходе реакций разложения из одного органического вещества образуются новые вещества. Например, при термическом крекинге бутана образуется этан и этен. Таким образом, разорвались углерод-углеродные связи и образовался алкан и алкен.
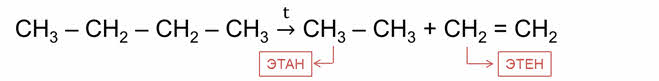
Реакциями изомеризации называются реакции превращения данного органического вещества в его изомер. Например, в реакции изомеризации пентана образуется его изомер – 2-метилбутан.
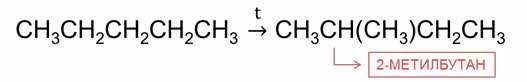
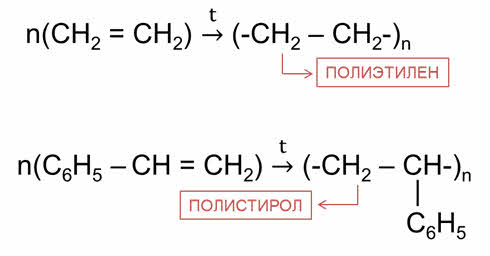
Особым видом органических реакций являются реакции полимеризации и реакции поликонденсации. Так, в реакции полимеризации этилена образуется полиэтилен.
В реакции полимеризации стирола – полистирол.
В реакции поликонденсации6-аминогексановой кислоты образуется капрон и низкомолекулярное вещество – вода. Примером реакции поликонденсации служит также реакция получения крахмала из глюкозы.
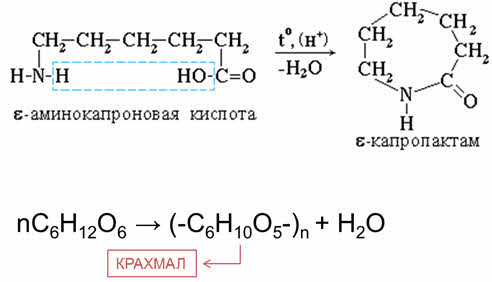
С участием кислорода или водорода проходят реакции окисления и восстановления. При этом происходит изменение степеней окисления. Так, при окислении этаналя гидроксидом меди (II) образуется этановая кислота. При этом степень окисления углерода меняется от +1 до +3. При восстановлении уксусного альдегида в присутствии никелевого катализатора образуется спирт – этанол. Степень окисления углерода изменяется с +1 до -1.
Таким образом, классифицировать химические реакции можно по различным признакам. Химические реакции сопровождаются разрывом одних связей и образованием других связей.
| <== предыдущая лекция | | | следующая лекция ==> |
| Методы ценообразования на основе себестоимости | | | Типология обществ по типу политического режима. Выделяют демократическое, авторитарное, тоталитарное общество. |
Дата добавления: 2021-10-28; просмотров: 152;










