Химические процессы. Виды технологических процессов
Классификация химических процессов:
По параметрам производства (высокотемпературные, низкотемпературные, некаталитические, каталитические, проходящие под повышенным или пониженным давление, электрохимические, биохимические, радиационно-химические, плазмохимические, фотохимические и т.д.)
По направлению движения тепловых и материальных потоков (прямоточные, противоточные, процессы с перекрестным и смешенным ходом)
По агрегатному состоянию (гомогенные и гетерогенные)
По тепловому эффекту (экзотермические, эндотермические)
Процесс химического превращения:
1.Подвод реагирующих компонентов в зону реакции
2. Химическая реакция
3. Отвод полученных продуктов из зоны реакции
Характер химического процесса:
1.Диффузионный
2. Кинетический
3. переходный
Выход продукта:
Х=Мф/Мт – выход продукта
Хр=Мр/Мт – равновесный выход продукта
Хф=(Мф/МтМр)100% - фактический выход продукта
Виды технологических процессов
1. Высокотемпературные процессы - «Металлургия – высотемпературная химия»ипирогенная переработка топлива, например, фракционная перегонка нефти.
2. Электрохимические процессы – процессы, основанные на непосредственном переходе электрической энергии в химическую без промежуточного этапа превращения энергии в теплоту. В качестве примера рассмотрим электрохимическое производство хлора. Основным промышленным методом получения хлора является электролиз концентрированного раствора NаС1. Принципиальная схема электролизера показана на рис.1 (А - аноды, Б - диафрагма, В - катод). При электролизе на аноде выделяется хлор, а в при катодном пространстве выделяется водород образуется NаОН. При практическом осуществлении электролиза раствора NaCl расход электроэнергии на получение 1 т хлора составляет около 2700 кВт·ч. Полученный хлор под давлением сгущается в желтую жидкость уже при обычных температурах. Хранят и перевозят его в стальных баллонах, где он заключен под давлением около 6 атм. Баллоны эти должны иметь окраску защитного цвета с зеленой поперечной полосой в верхней части.
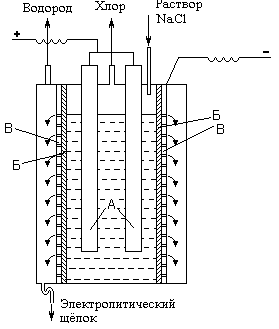
Рис. 1. Электрохимическое производство хлора
3. Биохимические процессы основаны натехническом использовании биохимических процессов, протекающих в живой клетке. Микробиологическая промышленность - отрасль промышленности, в которой производственные процессы базируются на микробиологическом синтезе ценных продуктов из различных видов непищевого сырья (углеводородов нефти и газа, гидролизатов древесины), а также отходов промышленной переработки сахарной свёклы, кукурузы, масличных и крупяных культур и т. д. Выпускает белково-витаминные концентраты, аминокислоты, витамины, ферментные препараты, антибиотики, бактериальные и вирусные препараты для защиты растений от вредителей и болезней, бактериальные удобрения, а также продукты комплексной переработки растит, сырья - фурфурол, ксилит и др. . Микробиологическая промышленность возникла в ходе НТР и основана на новейших достижениях микробиологии, химии, физики, химических технологий и кибернетики. На научной основе создаются всё более совершенные инженерно-биологические системы, в которых свойственная микроорганизмам огромная энергия ферментативного превращения веществ используется для направленного синтеза продуктов, необходимых сельскому хозяйству и промышленности. Значительная часть продукции микробиологической промышленности употребляется для получения биологически полноценных комбикормов. В расчёте на 1 m дрожжей, добавленных в корма, на фермах дополнительно производится до 800-1200 кг свинины, или 1500-2000 кг мяса птицы (в живом весе), или 15-25 тыс. яиц, сберегается 3,5-5 т зерна. Экономическая эффективность животноводства ещё более возрастает, когда вместе с кормовыми дрожжами в состав рационов вводятся недостающие витамины и аминокислоты, кормовые антибиотики, ферментные препараты.
Повышению урожайности полей, огородов, садов и виноградников способствуют микробиологические средства для борьбы с вредителями и возбудителями болезней растений, а также бактериальные удобрения. Микробные и вирусные инсектициды безопасны для человека, полезных животных и насекомых, помогают охране природы и улучшают условия воспроизводства в растительном и животном мире.
Ферментные препараты намного ускоряют ряд технологических процессов обработки с.-х. сырья, повышают выход и улучшают качество продукции в пищевой, мясной, молочной и лёгкой промышленности, значительно увеличивают производительность труда. Ферментные препараты применяются также в химической промышленности (выпуск моющих средств высокого качества), перспективно использование их в чёрной металлургии (удаление жира с тонкокатаного стального листа), в системах очистки промышленных и бытовых сточных вод.
4. Фотохимические процессы. Фотохимия изучает химические реакции, протекающие под действием света или вызываемые им. Механизм основан на активации молекул реагирующих веществ при поглощении света. Стадии фотохимической реакции: поглощение света и переход молекулы в возбужденное состояние, первичные химические процессы, вторичные реакции веществ, образовавшихся в первичном процессе
5.Радиационно-химические процессы. Стадии: физическая, физико-химическая и химическая. Направления применения РХП в промышленности: радиационная полимеризация, радиационное сращивание полимеров, радиационно-химический синтез, радиационное модифицирование неорганических материалов, радиационная очистка.
Основные понятия химической технологии. Предмет и задачи химической технологии
Химическая технология - наука о методах и процессах массовой переработки сырья в продукты потребления и средства массового производства. Химическая технология изучает процессы, связанные с коренным изменением состава и структуры вещества, осуществляемые путем химических реакций. Первой основной задачей химической технологии является исследование и установление оптимальных условий осуществления химических реакций на производстве, т.е. условий при которых химические реакции протекают с максимальным экономическим эффектом, с наилучшими технико-экономическими показателями. В химической технологии подбираются оптимальные концентрации реагирующих веществ, температура, давление, катализаторы, скорость протока и т.д. Производство любого химического продукта состоит из ряда механических, химических, физико-химических процессов, совокупность которых составляет технологическим процесс, который складывается из связанных между собой элементарных процессов:
1)подвод реагентов в зону реакции (совершается молекулярной диффузией или конвекцией. При сильном перемешивании реагирующих веществ конвективный перенос называют турбулентной диффузией. В двух или многофазных системах подвод реагирующих компонентов может совершаться абсорбцией, адсорбцией или десорбцией газов, конденсацией паров, плавлением твердых веществ, растворением твердых веществ);
2)химическое взаимодействие реагирующих веществ (в реагирующей системе обычно происходит несколько последовательных или параллельных химических реакций, приводящих к образованию основного продукта, а так же ряд побочных химических реакций между основными веществами и примесями, встречающимися в исходном сырье. Обычно при анализе производственных процессов учитываются не все реакции, а только те из них, которые имеют определяющее влияние на качество и количество получаемых целевых продуктов);
3) отвод продуктов из зоны реакции (Процесс может осуществляться также как и подвод реагирующих компонентов диффузией, конвекцией, переходом вещества из одной фазы в другую).
Технологический процесс химического производства делится на основные стадии. За основу стадии производства принмается определенная химическая реакция или физико-химический процесс, для протекания которых подбираются оптимальные условия. Выделение и установление стадий технологического процесса является второй основной задачей химической технологии. Последовательное графическое изображение процесса переработки исходных веществ в продукты производства и используемых в процессе аппаратов и машин, называется технологической схемой производства. В химической промышленности используют различные виды технологических схем, которые можно классифицировать по трем принципам:
1. По принципу осуществления производственного процесса во времени технологические процессы делятся на
а)периодические (весь процесс и каждая стадия производства осуществляются с перерывами - загрузка сырья в
аппарат, проведение процесса переработки сырья, выгрузка
готового продукта; затем цикл повторяется);
б) непрерывные (подача сырья, отбор продуктов и
весь процесс производства проводится непрерывно);
в) комбинированные (представляют собой сочетание
непрерывного и периодического процессов).
Непрерывные процессы имеют ряд преимуществ, поэтому в химической промышленности сложилась тенденция перехода от периодических и комбинированных процессов к непрерывным.
2. По принципу взаимного перемещения реагирующих веществ или тепловых потоков процессы делятся на:
а) прямоточные или параллельноточные (с движением реагирующих веществ или тепловых потоков в одно направлении);
б) противоточные (с движением реагирующих веществ или тепловых потоков навстречу друг другу);
в) перекрестные (с движением потоков под тем или иным углом друг к другу)
Противоточные процессы имеют ряд преимуществ.
3. По принципу достижения полноты протекания обратимых реакций схемы делятся на:
а) схемы с открытой цепью (полнота протекания обратимой реакции достигается многократным пропусканием не прореагировавших веществ черезпоследовательно установленные однотипные аппараты);
б) циклически, или круговые (не прореагировавшие вещества возвращаются в реакционный аппарат, предварительно смешиваясь со свежими порциями исходных веществ);
4. По агрегатному состоянию взаимодействующих веществ соответствующие им процессы делятся на:
а) однородные (гомогенные) (все реагирующие вещества находятся в одной какой-либо фазе);
б) неоднородные (гетерогенные) (системы включают
две или большее количество фаз)
5. По гидродинамическому режиму различают
два предельных случая перемешивания реагирующих компонентов с продуктами реакции:
а) полное смешение (турбулизация настолько сильна, что концентрация реагентов в проточном реакторе одинакова во всем объеме аппарата от точки ввода исходной смеси до вывода продукционной смеси);
б) идеальное вытеснение (исходная смесь не перемешивается с продуктами реакции, а проходит ламинарным потоком по всей длине или высоте аппарата)
6. По температурному режиму проточные реакторы и процессы, происходящие в них, делят на:
а) изотермические (температура постоянна во всем
реакционном объеме);
б) адиабатические (отсутствует отвод или подвод тепла, вся теплота реакции аккумулируется потоком реагирующих веществ);
в) политермические (программно-регулируемые) (в таких реакторах тепло реакции частично отводится из зоны реакции или компенсируется подводом для эндотермических процессов в соответствии с расчетом аппарата.
Исходя из классификации процессов, вытекает третья задача химической технологии – обоснованный выбор технологической схемы производства, дающий наибольший экономический эффект. На основе выбранной технологической схемы проектируется и рассчитывается аппаратура, обеспечивающая непрерывность процесса и получение целевого продукта в необходимом количестве и высокого качества. Это - четвертая задача химической технологии.
Все процессы, протекающие при производстве химической продукции, подчиняются общим законам материального мира, характеризуются общностью явлений, лежащих в их основе. Поэтому химическая технология использует материалы ряда других наук: математики, механики, физики, комплекса инженерных наук, химических наук, минералогии и др. Эти науки можно считать дисциплинами, обеспечивающими химическую технологию. В тоже время сама химическая технология составляет основу экономических наук, изучающих химическое производство. Ее материалы используются при изученииэкологических проблем. Эти дисциплины относятся к обеспечиваемым химической технологией.
Основываясь на базе различных наук, химическая технология широко использует соответствующие закономерности и терминологию. Основные принципы и обобщения физической химии в химической технологии используют для определения направления технологических процессов, выбора оптимальных условий, технологической схемы, аппаратного оформления производства. Физико-химические константы рассматриваются как предельные закономерности, к достижению которых стремится химическая технология. В химической технологии большая часть материальных и тепловых расчетов основана на стехиометрических уравнениях реакций. Однако производственные технологические расчеты значительно сложнее, т.к. приходится учитывать не только количественные соотношения реагирующих масс, но состав сырья, готовой продукции и выход продукта.
Химическая промышленность строится и развивается на глубоко научной основе, широко использует все новейшие достижения науки и техники. Под научными основами химической технологии следует понимать общие законы физики, химии и технических наук, лежащие в основе химических производств.
Из законов физики и химии выделяются два закона: закон сохранения массы вещества и закон сохранения энергии, на основе которых в химической технологии производят расчеты технологических процессов. Например, вычисляют тепловой и материальный балансы производства, выход готовой продукции, количество необходимого сырья и т.д.
В основе множества химико-технологических процессов лежат обратимые реакции. Протекание обратимых реакций определяется законом действующих масс, законом Ван-Гоффа и принципом Ле-Шателье.
Закон действующих масс устанавливает взаимосвязь между скоростью химической реакции и концентрацией реагирующих веществ. Как следствие из закона действия масс вытекает ряд технологических приемов. Например, для повышения скорости реакции и смещения равновесия обратимых реакций в сторону образования готовых продуктов используют концентрированные растворы и систематически досыщают их в процессе производства, а так же применяют повышенные и высоким давления ( при протекании обратимых реакций в газовой фазе); отводят продукты реакции из гетерогенной системы реагирующих веществ и т.д.
Закон Ван-Гоффа устанавливает взаимосвязь между температурой и направлением течения обратимых реакций. Он формулируется следующимобразом: если температура системы, находящейся в равновесии, изменяется, то при повышении температуры равновесие смещается в сторону процессов идущих с поглощением тепла, а при понижении температуры - в сторону процессов, идущих с выделением тепла. В зависимости от того, как протекает процесс, производят охлаждение или нагревание реагирующей системы.
Названные два закона представляют собой частные случаи общего закона, известного под названием принципа Ле-Шателье. Применительно к химическому равновесию этот принцип можно сформулировать так: если в равновесной системе изменить одно из условий равновесия температуру, давление, концентрацию реагирующих веществ), то равновесие смещается в направлении той реакции, которая ведет к ослаблению влияния произведенного изменения. Принцип Ле-Шателье является теоретической основой для выбора оптимальных условий, позволяющих наиболее экономично использовать сырье и обеспечивать максимальный выход готовой продукции заданного качества.
В химической технологии используют и другие законы физики и химии:
- газовые законы – для приведения объемов реагирующих газов к нормальным условиям и расчета технологических процессов, протекающих в газовой фазе либо с образованием газа;
- для расчета протекания электрохимических процессов используют законы электролиза;
-для расчетов экзо- и эндотермический процессов используют термохимические законы.
Наряду с законами природы химическая технология использует закономерности инженерных и экономических наук, которые можно назвать политехническими принципами. К числу таких научных принципов химической технологии относятся:
1. принцип непрерывности технологических процессов
2. принцип комплексной механизации и автоматизации
3. принцип комплексного использования сырья
4. принцип специализации, кооперирования, комбинирования производства
5. принцип соответствия аппаратуры протекающим в ней процессам
6. принцип противотока в технологических процессах
7. принцип цикличности технологических процессов
8. принцип регенерации веществ и энергии в технологических процессах.
Обобщенный образ технологической системы
Для оценки эффективности функционирования конкретной технологической системы независимо от уровня ее сложности (отдельный аппарат, установка, агрегат в составе производства или производство в целом) целесообразно воспользоваться моделью «черного ящика» с сосредоточенными входами и выходами потоков вещества и энергии. Пусть в системе за каждый технологический цикл – при периодическом режиме работы установки, либо в течение произвольного конечного временного интервала – в стационарном режиме, происходит преобразование массы m исходных веществ, взятых в определенной пропорции, в известные конечные продукты и отходы технологического процесса, масса которых сохраняется равной массе исходных веществ. В ходе процесса выделенная порция исходных веществ переводится из некоторого начального термодинамического состояния „1”в конечное термодинамическое состояние „ 2 ”. Здесь подразумевается, что как начальное, так и конечное состояния вещества характеризуются достаточно полной совокупностью физико-химических параметров каждого из отдельных материальных потоков, соответственно поступающих и выходящих из системы (химический состав, давление, температура и т.д.).
Так, современный агрегат производства азотной кислоты преобразует суммарный поток исходных веществ – жидкого аммиака, воздуха, питающей воды и природного газа (последний используется в качестве реагента для нейтрализации остаточных количеств оксидов азота на выхлопе установки) суммарный поток конечных продуктов – концентрированной азотной кислоты (целевой продукт), водяного пара (сопродукт) и сбросовых газов (отходы производства) – см. рис. 2. Химическое преобразование материальных потоков в установке получения азотной кислоты из аммиака сопровождается значительным по величине переходом энергии из одной формы в другую: высокопотенциальная химическая энергия аммиака и природного газа превращается в тепловую энергию водяного пара и в теплоту, рассеиваемую в окружающую среду.
Тепловая электростанция, работающая на природном газе, преобразует потоки газа, воздуха и питающей воды в материальные потоки водяного пара и дымовых газов и в поток электрической энергии(рис. 3).
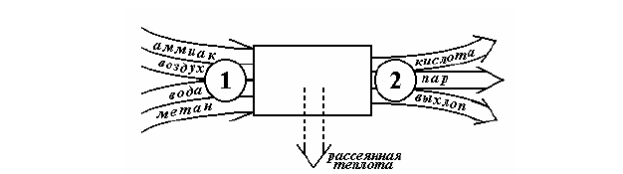
Рис. 2. Входящие и выходящие потоки в установке для получения азотной кислоты из аммиака; 1и 2обозначают начальное и конечное состояния совокупного материального потока через установку.
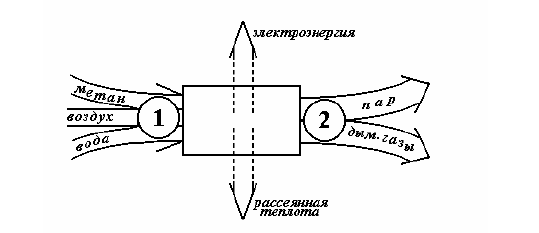
Рис. 3. Входящие и выходящие потоки на тепловой электростанции
Информация о химическом составе и термодинамических параметрах материальных потоков на входе и выходе системы плюс информация о суммарных потоках энергии в виде теплоты или работы, потребляемых (или генерируемых) системой, вполне достаточна, чтобы интегральным образом охарактеризовать эффективность ее функционирования как в отношении полноты использования сырьевых материалов (степени их превращения в целевые продукты), так и в отношении рационального потребления энергоресурсов. Интегральные, основанные на параметрах входов и выходов, характеристики систем играют в технологии двоякую роль. Во-первых, они позволяют ранжировать разнообразные варианты решений одной и той же технологической задачи по эффективности использования материальных и энергетических ресурсов. Во-вторых, поскольку фундаментальные законы природы накладывают строго определенные ограничения на полноту протекания взаимных превращений веществ и форм энергии, интегральные характеристики технологической системы достаточны для того, чтобы, отвлекаясь от всех деталей ее внутренней структуры и механизмов функционирования, оценить степень приближения реальной системы к гипотетическому, но разрешенному законами природы пределу. Такого рода оценки позволяют установить имеющиеся резервы для дальнейшего совершенствования технологических систем различного назначения с целью сбережения природных ресурсов.
Для теории энергосберегающих технологий основополагающее значение имеет следующая постановка вопроса. Пусть некоторая совокупность исходных веществ, природного происхождения или промышленных полупродуктов, перерабатывается в определенные целевые химические продукты и неизбежные производственные отходы. Другими словами, пусть некоторый совокупный материальный поток из исходного состояния „1”преобразуется в известное конечное состояние „ 2 ”(как это схематически показано на рис.2 и 3). Можно ли указать такие траектории проведения процесса 1→2, т.е. такие последовательности промежуточных состояний перерабатываемого вещества при его переходе из состояния 1в состояние 2, которым отвечает наиболее эффективное использование как энергии от внешних источников, так и собственной внутренней энергии исходных реагентов? Термодинамика положительно отвечает на этот вопрос, одновременно предлагая и универсальный критерий эффективности использования энергоресурсов различной природы. Можно сказать, что, в свою очередь, задачей технологии как самостоятельной науки является разработка способов реализации траекторий, близких к оптимальным в указанном смысле.
Дата добавления: 2021-09-25; просмотров: 427;










