Законы стехиометрии
Основные законы стехиометрии, включающие законы количественных соотношений между реагирующими веществами с помощью уравнений химических реакций, вывод формул химических соединений, составляют раздел химии, называемый стехиометрией.Стехиометрия включает в себя законыАвогадро,постоянства состава, кратных отношений, Гей-Люссака, эквивалентов и сохранения массы.
В основу составления химических уравнений положен метод материального баланса, основанный на законе сохранения массы (М.В. Ломоносов, 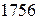 , А. Лавуазье,
, А. Лавуазье,  ).
).
Закон сохранения массы веществ: масса всех веществ, вступивших в химическую реакцию, равна массе всех веществ, образовавшихся в результате реакции.
В химической реакции число взаимодействующих атомов остаётся неизменным, происходит только их перегруппировкас разрушением исходных веществ. Взаимодействие водорода и кислорода с образованием воды может быть записано с помощью уравнения химической реакции

Коэффициенты перед формулами химических соединений называются стехиометрическими.
Закон постоянства состава(Ж. Пруст) Каждое индивидуальное химическое вещество имеет постоянный качественный и количественный состав и определённое химическое строение независимо от способа его получения.
Такие соединения называются дальтонидами или стехиометрическими в отличие от бертолидов, состав которых зависит от способа получения. Они состоят не из молекул, а из атомов или ионов.
Закон кратных отношений(Д. Дальтон) Если два элемента образуют между собой несколько молекулярных соединений, то масса одного элемента, приходящаяся на одну и ту же массу другого, относятся между собой как небольшие целые числа.
Пусть у нас имеются данные о процентном содержании азота и кислорода в трёх оксидах:  . Рассчитаем, сколько весовых частей кислорода приходится на одну весовую часть азота в этих соединениях: в
. Рассчитаем, сколько весовых частей кислорода приходится на одну весовую часть азота в этих соединениях: в  Между собой эти величины относятся как
Между собой эти величины относятся как 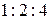 . Можно было бы таким же образом рассчитать весовые части азота, приходящиеся на одну весовую часть кислорода в этих оксидах. Взяв их отношения, мы получаем
. Можно было бы таким же образом рассчитать весовые части азота, приходящиеся на одну весовую часть кислорода в этих оксидах. Взяв их отношения, мы получаем  .
.
Закон эквивалентов(И. Рихтер) В молекулярных соединениях массы составляющих их элементов относятся между собой как их эквиваленты или массы взаимодействующих веществ пропорциональны их молярным массам эквивалентов 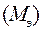 :
:
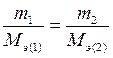 ,
, 
где 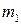 и
и  – массы реагирующих веществ, г, кг,
– массы реагирующих веществ, г, кг,
 и
и  – молярные массы эквивалентов этих веществ,
– молярные массы эквивалентов этих веществ, 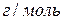 ;
; 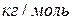 .
.
Химическим эквивалентом веществаназывается такое его количество, которое соединяется с  атомов водорода или замещает то же количество атомов водорода в химических реакциях. Это безразмерная величина.
атомов водорода или замещает то же количество атомов водорода в химических реакциях. Это безразмерная величина.
Моль эквивалентов –количество вещества, содержащего столько же структурных единиц, сколько их содержится в 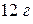 изотопа углерода
изотопа углерода 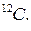
Массу одного моля эквивалента называют молярной массой эквивалента вещества 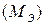 . Молярные массы эквивалентов веществ измеряют в
. Молярные массы эквивалентов веществ измеряют в 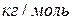 .
.
Поскольку молярная масса какого-либо вещества численно совпадает с его относительной молекулярной массой, то из закона эквивалентов можно вывести следующие формулы для вычисления эквивалентных масс простых и сложных веществ:
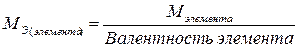 ,
, 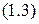
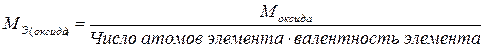 ,
, 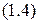
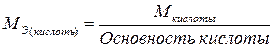 [2],
[2], 
 [3],
[3], 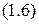
 .
. 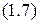
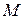 – мольная масса соединений,
– мольная масса соединений, 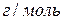 .
.
При решении некоторых задач, в условиях которых содержаться сведения об объёмах газообразных участников реакции, целесообразно пользоваться значением эквивалентного объёма.
Эквивалентным объёмом  называется объём, занимаемый при данных условиях
называется объём, занимаемый при данных условиях 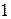 эквивалентом вещества. Значение эквивалентного объёма вещества, находящегося в газообразном состоянии, можно найти, зная, что в мольном объёме любого газа, состоящего из одноатомных молекул, содержится
эквивалентом вещества. Значение эквивалентного объёма вещества, находящегося в газообразном состоянии, можно найти, зная, что в мольном объёме любого газа, состоящего из одноатомных молекул, содержится 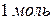 атомов, состоящего из двухатомных молекул –
атомов, состоящего из двухатомных молекул – 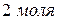 атомов и т.д. Например, в
атомов и т.д. Например, в 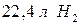 содержится при нормальных условиях4
содержится при нормальных условиях4 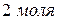 атомов водорода. Поскольку эквивалент атомов водорода равен
атомов водорода. Поскольку эквивалент атомов водорода равен 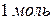 , то в
, то в 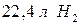 содержится
содержится 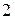 эквивалента атомов водорода. Следовательно, эквивалентный объём молекул
эквивалента атомов водорода. Следовательно, эквивалентный объём молекул 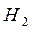 равен
равен 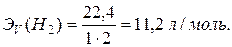 Рассуждая аналогично, вычислим эквивалентный объём газообразного кислорода
Рассуждая аналогично, вычислим эквивалентный объём газообразного кислорода 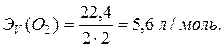
Дата добавления: 2016-06-05; просмотров: 2498;










