Влияние температуры на селективность
Влияние температуры на селективность связано с типом модели реактора. Т. к. реакторы смешения работают в изотермическом режиме, а реакторы вытеснения имеют либо адиабатический режим, либо политермический..
Влияние температуры выражается уравнением Аррениуса
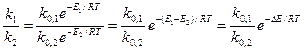 ,
,
где k0 – предэкспоненциальный множитель;
Е1, Е2 – энергии активации основной и побочной реакции.
Влияние температуры на селективность зависит от соотношения энергий активации параллельных реакций. Если энергия активации основной реакции выше Е1 > Е2 , то при низких температурах скорость побочной реакции выше, чем основной. Поэтому при низкой температуре селективность мала. Повышение температуры приводит к росту скорости и увеличению селективности. Если же Е1 < Е2 , то повышение температуры нецелесообразно.
В зависимости от соотношения Е1 и Е2 влияние температуры на селективность различно. Изменить это соотношение можно проведением процесса в присутствии селективного катализатора, который будет снижать энергию активации целевой реакции и мы будем получать высокий выход при низкой температуре.
Для РИС – Н величины Х, ФR и φ во всем объеме постоянны и поэтому связь между этими параметрами можно выразить уравнением
Ф = φ χ
Для РИВ эти же величины меняются по длине реактора, поэтому для него применяют выражение 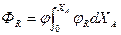
Графическое изображение этих уравнений позволяет установить тип реактора, обеспечивающий максимальный выход целевого продукта.
Для параллельных реакций 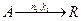
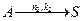
Селективность можно выразить уравнением
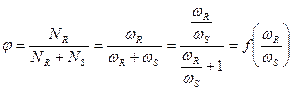 ,
,
т.е. является функцией отношения ωR/ωS .
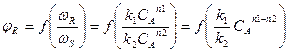
Из уравнения следует, что по постоянной температуре в каждом конкретном случае, когда известен порядок основной и побочной реакции, селективность зависит только от концентрации СА, так как отношение констант скорости реакции k1/k2 в этих условиях постоянная. Поэтому в зависимости от разности n1 – n2 влияние СА на φR может быть либо положительным, либо отрицательным.
1) Если порядок основной реакции выше порядка побочной реакции, т.е. n1 > n2 , то n1 – n2 = а.
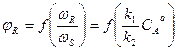
Т. е. при увеличении концентрации исходного вещества СА селективность возрастает. Следовательно, для достижения высокой селективности выгодно поддерживать высокую концентрацию исходного вещества, т.е. выгодно применять РИВ или К – РИС, т.к. в этих реакторах средняя концентрация реагента СА выше, чем в
РИС – Н.
2) Если порядок основной реакции ниже порядка побочной реакции, т.е. n1 < n2 то n1 – n2 = -а.
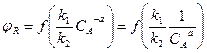
Из этого уравнения видно, что при увеличении СА селективность снижается. При этом выгодно применять РИС – Н, т. к. концентрация исходного вещества в нем ниже, чем в РИВ. В данном случае изменение величины СА оказывает на эти параметры противоположное действие (интенсивность и селективность). При снижении СА интенсивность уменьшается, а селективность возрастает. Что лучше – можно решить технико – экономическим анализом.
Если n1 = n2 , то n1 – n2 = 0
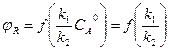 ,
,
т.е. селективность не зависит от концентрации исходного реагента и тип реактора не влияет на селективность. В этом случае изменяют температуру или применяют катализатор селективного действия, который может изменить соотношение k1/k2 .
Дата добавления: 2017-01-08; просмотров: 2422;










