Это основное уравнение кинетики ферментативной реакции - Михаэлиса-Ментен
Данное уравнение имеет несколько решений:
1. [S] >> KS; тогда величиной KS можно пренебречь и v = Vmax, пока концентрация субстрата велика, скорость реакции близка к максимальной и практически мало изменяется до тех пор, пока уменьшение концентрации субстрата не будет значительным. Реакция будет иметь нулевой порядок (n = 0).
2. [S] << KS; тогда практически скорость реакции будет описываться уравнением
Vmax
v = ------ [S],
KS
где Vmax и KS – кинетические константы и данное уравнение – уравнение прямой линии; скорость ферментативной реакции пропорциональна концентрации субстрата. Это реакция первого порядка (n = 1).
3. Величина [S] – промежуточная; пусть [S] = KS, v = 1/2Vmax. В данном случае порядок реакции будет дробный (0 < n <1).
Графическое решение уравнения

|
|
|
|


|
|
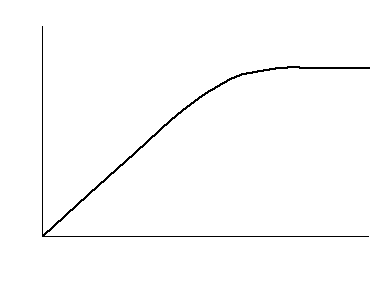
Таким образом, в ферментативных реакциях порядок реакции меняется в ходе самой реакции. При n = 0 не наблюдается дальнейшего увеличения скорости ферментативной реакции, т.к. произошло насыщение фермента субстратом. В неферментативных химических реакциях порядок от её начала до конца практически не меняется.
Уравнение Михаэлиса-Ментен справедливо для начала ферментативной реакции, когда в реагирующей смеси мало продуктов реакции. Дж. Бриггс и Дж. Холдейн модифицировали уравнение Михаэлиса-Ментен, они исходили из следующего уравнения ферментативной реакции:
k1 k2


 E + S ES Е + P
E + S ES Е + P
k-1
В этом ранении учитывается распад комплекса ES на Е и P, введя константу распада k2. Тогда
Vmax [S]
v = ----------
Km + [S]
Кm = (k-1 + k2)/ k1 – константа Михаэлиса – это концентрация субстрата, при которой скорость реакции составляет половину максимальной. Величина Кm характеризует фермента к субстрату. Чем меньше величина Кm тем больше сродство фермента к данному субстрату.
Дата добавления: 2016-12-09; просмотров: 2357;










