ЯТРОГЕННЫЕ НАРУШЕНИЯ ГЕМОСТАЗА
Врач должен помнить о том, что многие лекарственные препараты обладают прямым или косвенным воздействием на механизмы гемостаза.
В ряде случаев они используются целенаправленно, для коррекции гемостаза, в других обстоятельствах их действие проявляется как побочный эффект или осложнение.
Постоянно следует учитывать ту тенденцию, которая формируется этим медикаментозным, или другим вариантом воздействия на равновесное состояние механизмов гемостаза, и понимать, что в конечном итоге это воздействие может привести либо к гипокоагуляции, либо к гиперкоагуляции, либо к тому и другому одновременно, что ещё хуже.
Действие на плазменную систему свёртываемости крови оказывают:
– антикоагулянты непрямого воздействия (кумарины, фенилин, варфарин), которые создают дефицит К-зависимых факторов – гипокоагуляция.
– антикоагулянты прямого действия – компоненты антисвёртывающей системы: гепарин;
– избыток введённого извне цитрата при «синдроме массивной гемотрансфузии». Хотя следует помнить, что дефицита Са++ в крови не оказывается даже при снижении его до уровня, вызывающего судорожный синдром.
Действие на фибринолитическую систему:
– активаторы фибринолиза – урокиназа, стрептокиназа, деказа;
– дефибринирующие препараты – делают из яда гремучих змей, способствуют образованию легко лизирующихся тромбов – гипокоагуляция;
– экзогенные ингибиторы фибринолиза – эпсилон-аминокапроновая кислота;
– антагонисты фибринолиза:
· трасилол и другие антипротеазы – гиперкоагуляция;
· ингибирование калинокреин-кининовой системы – гиперкоагуляция;
· тромболитины.
Действие на тромбоциты:
– ингибиторы образования тромбоксана-А2 или его функции угнетают адгезию и агрегацию. Это:
¨ противомалярийные препараты (хинакрин);
¨ простоциклин и его аналоги;
¨ имидазол, блокирующий тромбоксансинтетазу;
¨ большие дозы глюкокортикоидов;
¨ ингибиторы синтеза простаглодинов, воздействующие на циклооксигеназу:
v ацитилсалициловая кислота;
v индометацин;
v бруфен;
v бутадион;
v сульфопиразон;
– группа препаратов стимулирующих фосфорилирование, или другим способом повышающих концентрацию цАМФ (ингибиторы фосфодиэстеразы);
– повышенный уровень цАМФ – курантил, папаверин, никотиновая кислота, вазопрессин и т.д.
– блокаторы транспорта Са++: изоптин, коринфар.
Лекция № 21
Нарушения электрогенеза сердца. Механизмы формирования
элементов электрокардиограммы в норме и патологии.
Электрокардиографические изменения в условиях заболеваний сердца
Итак, напомню Вам, что координированная работа отделов сердца обеспечивается 4 основными свойствами сердечной мышцы: ВОЗБУДИМОСТЬЮ, АВТОМАТИЗМОМ, ПРОВОДИМОСТЬЮ, СОКРАТИМОСТЬЮ. Сегодня нас будут интересовать возбудимость, как базовое свойство миокарда, а так же автоматизм и проводимость.
Возбудимостью называется способность биологической системы под действием раздражителя изменять уровень обмена веществ, энергии и информации в виде специфической ответной реакции. Специфика возбудимости сердца была известна давно: еще в XVIII веке ученик Галлера Ф. Фонтана показал, что сердце может ответить, или не ответить на раздражение в зависимости от того, в какой промежуток времени после предыдущего сокращения наносится раздражение. Оказывается, после предыдущего сокращения сердечная мышца оказывается какое-то время невозбудимой. Эта особенность возбудимости миокарда, названная рефрактерностью, получила свое объяснение много позже, уже в 70-х годах нашего столетия – это сделал английский ученый Лилли. Если представить график потенциала действия типического кардиомиоцита (рис. 1), то обращает на себя внимание очень длительная фаза плато, которая по времени занимает всю механическую систолу и треть диастолы.
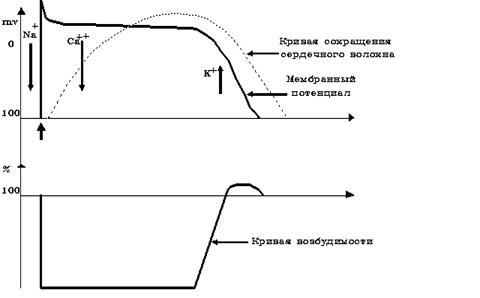
Рис. 1. Соотношение фаз возбудимости, потенциала действия
и кривой одиночного мышечного сокращения
типического волокна сердечной мышцы
Это необычное для скелетной мышцы явление, было объяснено Лилли, показавшим, что после развития пика деполяризации, активация калиевых каналов приводит к включению особого класса ионных каналов, обнаруженных только у сердечной мышцы и названных потенциал-независимыми, калий-зависимыми кальциевыми каналами. Входящий ток кальция во время реполяризации как бы задерживает потенциал мембраны на постоянном, но достаточном для активации натриевых каналов уровне, которые подвергаются постоянной инактивации, и как следствие – делают мембрану невозбудимой. Действительно, если посмотреть на кривую возбудимости мембраны, хорошо видно, что сердце практически невозбудимо во время систолы и части диастолы. Какое значение для сердечной мышцы имеет длительная рефрактерность? Основное значение – это препятствие к возникновению т.н. слитных или тетанических сокращений миокарда. Дело в том, что при таком типе сокращений нарушается фазная работа предсердий и желудочков, т.е. теряется насосная функция сердца. Нужно сказать, что, несмотря на такой надежный защитный механизм как рефрактерность, все же могут наблюдаться патологические нарушения возбудимости сердца, которые самым тяжелым образом отражаются на гемодинамике.
Одним из наиболее тяжелых проявлений таких нарушений является ТРЕПЕТАНИЕ ПРЕДСЕРДИЙ (частота их сокращений достигает 250 – 400 в 1 минуту). Желудочки при этом отвечают на вторую, третью или четвертую волну сокращений предсердий. Еще тяжелее нарушения при мерцании предсердий, когда число сокращений доходит до 400 – 600 в минуту, при этом нет единого сокращения и расслабления, а подвергаются сокращению отдельные волокна. Практически полное отсутствие кровообращения, утрата пропульсивной силы сердца наступает при ФИБРИЛЯЦИИ ЖЕЛУДОЧКОВ. Причин подобных тяжелых нарушений возбудимости чрезвычайно много: среди них особое значение имеют дисметаболические расстройства при действии ряда токсических веществ – хлороформ, циклопропан, гормональных нарушениях, гипокалийемии, при резкой гипоксии, при перегрузке или травме сердца, при отравлении наперстянкой и др. Всего же описано несколько сотен синдромов нарушения возбудимости, автоматии и проводимости миокарда, для понимания патогенеза развития которых, а главное для надежной диагностики, необходимо иметь представления о проявлениях электрической деятельности сердца.
Как вы понимаете, речь идет о клинических основах электрокардиографии. Когда у студента спрашиваешь, что же такое электрокардиография, то обычно получаешь ответ, что ЭКГ – это регистрация биопотенциалов сердца. Кстати, и некоторые учебные пособия примерно так же определяют ЭКГ. Однако в этом случае возникает вопрос: а зачем же в клинике используют другие электрографические методы исследования сердца, например субэндокардиальную электрографию? Действительно, кто даст катетеризировать свое сердце (довольно небезобидная процедура), устанавливать присасывающиеся электроды только для того, чтобы получить информацию, которую можно записать с поверхности тела? По-видимому, дело обстоит не так просто.
Для того чтобы разобраться в сути методики, полезно сделать небольшой экскурс в историю. То, что в сердце при возбуждении возникает разность потенциалов, было показано еще в 1856 г. учениками Дюбуа-Реймона – Келликером и Мюллером. Опыт был поставлен точно по рецептам Гальвани: на изолированное сердце лягушки клался нерв, идущий к лапке и этот «живой вольтметр» отвечал вздрагиванием лапки на каждое сокращение сердца лягушки. С появлением чувствительных электроизмерительных приборов стало возможным регистрировать и ЭКГ человека. Это впервые было сделано английским ученым А. Уоллером (1887) с помощью капиллярного электрометра. Основу этого прибора составлял тонкий капилляр, в котором ртуть граничила с серной кислотой; при пропускании тока через такой капилляр поверхностное натяжение на границе жидкостей менялось и мениск смещался по капилляру. Этот прибор был неудобен в использовании и широкое применение электрокардиографии началось позже, после появления в 1903 г. более совершенного прибора – струнного гальванометра В. Эйнтховена. Работа этого прибора основана на движении проводника с током в магнитном поле. Роль проводника играла посеребренная кварцевая нить диаметром в несколько микрометров, туго натянутая в магнитном поле. При пропускании по этой струне электрического тока она слегка изгибалась. Эти отклонения наблюдались с помощью микроскопа. Прибор обладал малой инерцией и позволял регистрировать быстрые электрические процессы. После появления этого прибора стали изучать, чем же отличается ЭКГ здорового человека и сердца при разных заболеваниях. За эти работы В.Эйнтховен в 1924 г. получил Нобелевскую премию, а русский ученый Самойлов, много сделавший для развития электрокардиографии, получил в 1930 году Ленинскую премию.
Ключевым вопросом теории ЭКГ являлся вопрос о природе возникающей ЭДС сердца. По мнению Эйнтховена, да и большинства последующих исследователей, появление диполя и электродвижущей силы (ЭДС) обусловлено ионными токами (входящими и выходящими из кардиомиоцитов), которые в силу относительно хорошей электропроводности жидких сред нашего тела, проходят на поверхность кожи, где и регистрируются. Действительно, при расположении электродов на поверхности сердца, амплитуда возникающих потенциалов достигает 120 мв (амплитуда потенциала действия типического кардиомиоцита). При регистрации ЭКГ с помощью подкожных электродов регистрируются потенциалы порядка 5 – 8 мв, а с помощью накожных – около 1 мв. Казалось бы, все ясно – идет затухание ионных токов в соответствии с удаленностью от источника ЭДС и сопротивлением тканей. Однако, как это часто бывает в науке, все карты спутал один казус. В конце 20-х годов в одной из лабораторий США лаборант, позабыв надеть электроды на пациента (электроды лежали рядом на кушетке), тем не менее, умудрился зарегистрировать ЭКГ. Проанализировав ситуацию, американцы пришли к выводу, что ЭКГ можно регистрировать и через воздушное пространство вокруг пациента. Позже, была предложена методика телеэлектрокардиографии, которая предполагала дистанционный съем и регистрацию ЭКГ. Поскольку воздух обладает бесконечно высоким сопротивлением для электрического тока, стало ясно, что при регистрации ЭКГ имеют дело с электрическим полем. Носителями зарядов при этом являются не относительно тяжелые ионы, а легкие электроны. Это позволяет определить электрокардиографию как методику регистрации напряженности электрического силового поля, создаваемого работающим сердцем. Происхождение этого поля довольно сложное, но доказано, что большое значение имеет электромагнитная индукция, возникающая при пересечении движущимися зарядами в сердце магнитных силовых линий Земли (т.н. «мультипольная» теория возникновения ЭКГ). Данный, казалось бы, мелкий штрих в конкретизации рассматриваемой методики, кардинально меняет наши представления о механизме возникновения зубцов, сегментов и интервалов ЭКГ.
 Рассмотрим этот механизм (рис. 2). В соответствии с теорией диполя Эйнтховена, сердце в начале возбуждения, в области синусного узла приобретает отрицательный заряд, в то время как остальные отделы миокарда заряжены положительно. Напомню, что положительный заряд наружной мембраны кардиомиоцита обусловлен потенциалом покоя – т.е. выходом ионов калия из клетки в невозбужденном состоянии. При возбуждении возникает вход ионов натрия и кальция внутрь клетки, приводящий к перезарядке мембраны – потенциал действия, мембрана становится заряженной отрицательно. Вокруг разных зарядов возникают электрические поля. Электрическое поле способно приводить в движение наиболее заряженные и подвижные частицы (с наиболее высоким удельным зарядом – электроны). Количество движущихся частиц в единицу времени (т.е. напряженность электрического поля) характеризуется разностью зарядов диполя (ЭДС), а направление – пространственной ориентацией зарядов по отношению друг к другу. Линии наибольшей напряженности электрического поля во время сердечного цикла характеризуют т.н. электрическую ось сердца – она, как правило, совпадает с анатомической осью сердца, т.к. движение возбуждения по проводящей системе направлено вдоль длинника сердца. Поскольку электроны имеют отрицательный заряд, электрическая ось сердца направлена сверху вниз и справа налево. Если рассматривать только фронтальную плоскость, то сердце можно вписать в равносторонний треугольник, вершинами которого являются две руки и левая нога пациента. Расставим полярность электродов у вершин треугольника. Поскольку, поток электронов направлен сверху вниз и справа налево, то очевидно, правая рука должна иметь преимущественно отрицательный заряд, а левая нога – преимущественно положительный. Соответственно, левая рука имеет переменный заряд: при I стандартном отведении, т.е. с правой рукой – положительный, а в III стандартном отведении, т.е. с левой ногой – отрицательный. На середине каждого отведения находится т.н. эквипотенциальная или нулевая точка, характеризующая минимальную напряженность электрического поля в данный момент или минимальное значение вектора электромагнитной индукции.
Рассмотрим этот механизм (рис. 2). В соответствии с теорией диполя Эйнтховена, сердце в начале возбуждения, в области синусного узла приобретает отрицательный заряд, в то время как остальные отделы миокарда заряжены положительно. Напомню, что положительный заряд наружной мембраны кардиомиоцита обусловлен потенциалом покоя – т.е. выходом ионов калия из клетки в невозбужденном состоянии. При возбуждении возникает вход ионов натрия и кальция внутрь клетки, приводящий к перезарядке мембраны – потенциал действия, мембрана становится заряженной отрицательно. Вокруг разных зарядов возникают электрические поля. Электрическое поле способно приводить в движение наиболее заряженные и подвижные частицы (с наиболее высоким удельным зарядом – электроны). Количество движущихся частиц в единицу времени (т.е. напряженность электрического поля) характеризуется разностью зарядов диполя (ЭДС), а направление – пространственной ориентацией зарядов по отношению друг к другу. Линии наибольшей напряженности электрического поля во время сердечного цикла характеризуют т.н. электрическую ось сердца – она, как правило, совпадает с анатомической осью сердца, т.к. движение возбуждения по проводящей системе направлено вдоль длинника сердца. Поскольку электроны имеют отрицательный заряд, электрическая ось сердца направлена сверху вниз и справа налево. Если рассматривать только фронтальную плоскость, то сердце можно вписать в равносторонний треугольник, вершинами которого являются две руки и левая нога пациента. Расставим полярность электродов у вершин треугольника. Поскольку, поток электронов направлен сверху вниз и справа налево, то очевидно, правая рука должна иметь преимущественно отрицательный заряд, а левая нога – преимущественно положительный. Соответственно, левая рука имеет переменный заряд: при I стандартном отведении, т.е. с правой рукой – положительный, а в III стандартном отведении, т.е. с левой ногой – отрицательный. На середине каждого отведения находится т.н. эквипотенциальная или нулевая точка, характеризующая минимальную напряженность электрического поля в данный момент или минимальное значение вектора электромагнитной индукции.
 Установив эти координатные точки, рассмотрим, как формируется нормальная ЭКГ, например в I стандартном отведении (рис. 3). Итак, представим, что мы соединили проводами электроды, расположенные на правой и левой руках с чувствительным регистратором. Предположим, что в сердце только что закончилась реполяризация желудочков, а возбуждение синусового узла еще не началось. Все кардиомиоциты имеют положительный заряд, что исключает возникновение пространственного диполя и электрического поля. Как мы условились, вектор электромагнитной индукции в этот момент равен нулю, следовательно, ЭДС самоиндукции в области электродов не возникает. Перо регистратора при этом не смещается от нулевой (изоэлектрической) линии. Как только возникает возбуждение синусной области, появляется очаг деполяризации ушка правого предсердия (отрицательный заряд), при этом формируется диполь с появлением вектора электромагнитной индукции, направленный справа налево. Проекция этого вектора на ось I отведения дает небольшой положительный вектор, который отклоняет стрелку вверх (все положительные значения ЭДС самоиндукции отклоняют перо вверх – возникают положительные зубцы, а отрицательные – вниз – отрицательные зубцы).
Установив эти координатные точки, рассмотрим, как формируется нормальная ЭКГ, например в I стандартном отведении (рис. 3). Итак, представим, что мы соединили проводами электроды, расположенные на правой и левой руках с чувствительным регистратором. Предположим, что в сердце только что закончилась реполяризация желудочков, а возбуждение синусового узла еще не началось. Все кардиомиоциты имеют положительный заряд, что исключает возникновение пространственного диполя и электрического поля. Как мы условились, вектор электромагнитной индукции в этот момент равен нулю, следовательно, ЭДС самоиндукции в области электродов не возникает. Перо регистратора при этом не смещается от нулевой (изоэлектрической) линии. Как только возникает возбуждение синусной области, появляется очаг деполяризации ушка правого предсердия (отрицательный заряд), при этом формируется диполь с появлением вектора электромагнитной индукции, направленный справа налево. Проекция этого вектора на ось I отведения дает небольшой положительный вектор, который отклоняет стрелку вверх (все положительные значения ЭДС самоиндукции отклоняют перо вверх – возникают положительные зубцы, а отрицательные – вниз – отрицательные зубцы).
Далее возбуждение охватывает все правое предсердие (проекция положительного вектора на ось I отведения увеличивается, перо еще больше отклоняется вверх). Следующий этап – возбуждение охватывает межпредсердную перегородку и далее переходит на левое предсердие. Обратите внимание на то, что направление вектора электромагнитной индукции при этом не меняется – он направлен справа налево, и, следовательно, продолжает формировать положительный зубец.
 Но, вот, наконец, оба предсердия охвачены возбуждением (рис. 4). Куда возбуждение движется затем? А никуда не движется – оно попросту стоит на месте. Это обусловлено сложной полисинаптической организацией узла Ашофа-Тавара, при этом возбуждение как бы замирает – это явление получило название атрио-вентикулярной задержки. Что же будет с вектором электромагнитной индукции – он начнет убывать и затем исчезнет совсем: это связано с тем, что электромагнитная индукция возникает только при пересечении магнитных силовых линий Земли движущимися зарядами сердца (пример с остановленным генератором). Как и следует ожидать, перо регистратора снова возвратится на изолинию. Так возникает первый элемент нормальной ЭКГ – зубец Р. Его часто называют предсердным, но как Вы видите это не совсем верно, т.к. Р отражает и возбуждение синоаурикулярной зоны и межпредсердной перегородки и самих предсердий, и самое главное – степень атриовентрикулярной задержки.
Но, вот, наконец, оба предсердия охвачены возбуждением (рис. 4). Куда возбуждение движется затем? А никуда не движется – оно попросту стоит на месте. Это обусловлено сложной полисинаптической организацией узла Ашофа-Тавара, при этом возбуждение как бы замирает – это явление получило название атрио-вентикулярной задержки. Что же будет с вектором электромагнитной индукции – он начнет убывать и затем исчезнет совсем: это связано с тем, что электромагнитная индукция возникает только при пересечении магнитных силовых линий Земли движущимися зарядами сердца (пример с остановленным генератором). Как и следует ожидать, перо регистратора снова возвратится на изолинию. Так возникает первый элемент нормальной ЭКГ – зубец Р. Его часто называют предсердным, но как Вы видите это не совсем верно, т.к. Р отражает и возбуждение синоаурикулярной зоны и межпредсердной перегородки и самих предсердий, и самое главное – степень атриовентрикулярной задержки.
Рассмотрим ход дальнейших событий (рис. 5). Пока длится атриовентрикулярная задержка, перо пишет прямую линию. Как только возбуждение проходит на проводящую систему желудочков, ситуация меняется. Проводящая система желудочков представлена вначале двумя ножками пучков Гиса, расположенными субэндокардиально по внутренней стороне межжелудочковой перегородки. Однако нужно учитывать анатомические особенности строения ножек. Левая ножка значительно толще и короче правой,  а, кроме того, имеет 2 ветви – переднюю и заднюю. Иными словами, сопротивление левой ножки меньше, чем правой и она значительно быстрее охватывается возбуждением, нежели правая. Посмотрите, к чему это приводит – в то время как левая половина межжелудочковой перегородки уже охвачена возбуждением, правая еще не возбуждена. При этом возникает дополнительный вектор ЭМИ, направленный слева направо и сверху вниз. При проецировании его на ось I отведения мы получаем небольшую, но отрицательную проекцию, т.е. перо регистратора отклонится вниз. Однако, в силу небольшой толщины межжелудочковой перегородки, очень скоро она будет охвачена возбуждением и отрицательный вектор исчезает. Перо вновь выходит на изолинию, а на ленте – сформирован первый зубец желудочкового комплекса – зубец Q (рис. 6). Это 1 фаза возбуждения желудочков.
а, кроме того, имеет 2 ветви – переднюю и заднюю. Иными словами, сопротивление левой ножки меньше, чем правой и она значительно быстрее охватывается возбуждением, нежели правая. Посмотрите, к чему это приводит – в то время как левая половина межжелудочковой перегородки уже охвачена возбуждением, правая еще не возбуждена. При этом возникает дополнительный вектор ЭМИ, направленный слева направо и сверху вниз. При проецировании его на ось I отведения мы получаем небольшую, но отрицательную проекцию, т.е. перо регистратора отклонится вниз. Однако, в силу небольшой толщины межжелудочковой перегородки, очень скоро она будет охвачена возбуждением и отрицательный вектор исчезает. Перо вновь выходит на изолинию, а на ленте – сформирован первый зубец желудочкового комплекса – зубец Q (рис. 6). Это 1 фаза возбуждения желудочков.

Затем, возбуждение идет по ветвям пучков Гиса и волокнам Пуркинье. При этом направление векторов ЭМИ расходится «веером» – и на верхушку и на основание правого и левого желудочков (рис. 7). Как из такого обилия векторов построить один, результирующий? Здесь имеют значение 2 обстоятельства:

1) сердце асимметрично расположено в грудной клетке – верхушкой ориентировано влево;
2) мощность левого желудочка примерно в 3-4 раза больше мощности правого.
Поэтому результирующий вектор ЭМИ будет иметь значительную величину и ориентирован сверху вниз и справа налево.
Проекция на I отведение даст большой положительный момент, и перо резко поднимется вверх. Поскольку, желудочки имеют очень развитую проводящую систему, охват возбуждением желудочков скоро будет завершен и этот вектор исчезнет. Перо вернется на изолинию и сформирует самый большой зубец ЭКГ – R (рис. 8). Это вторая фаза возбуждения желудочков.

Однако процесс охвата возбуждением желудочков на этом, как правило, не заканчивается: поскольку левый желудочек имеет большую массу, нежели правый, к моменту полного охвата возбуждением последнего, в левом остается невозбужденной еще зона основания желудочка. Для ее довозбуждения требуется дополнительный вектор, идущий снизу вверх и слева направо (рис. 9). Отрицательная проекция этого вектора отклоняет перо вниз, а по завершении охвата возбуждением и основания сердца формируется отрицательный зубец S (рис. 10). Это третья фаза возбуждения желудочков.

После завершения охвата возбуждением желудочков, все участки миокарда деполяризованы (электроотрицательны). Как Вы помните, процесс деполяризации в кардиомиоцитах (в отличие от скелетной ткани) как бы «застывает» благодаря фазе плато (см. рис. 1). Поэтому вслед за зубцом S наблюдается изолиния, длительность которой соответствует длительности фазы плато ПД. Это, собственно 4 фаза возбуждения желудочков. Как только эта фаза заканчивается, в клетках сердца развивается реполяризация. Следует подчеркнуть, что развитие реполяризации в желудочках начинается в самой дистальной по отношению к проводящей системе части сердца, а именно – субэпикардиальных слоях миокарда (рис. 11). Эти слои быстрее всего выходят из состояния рефрактерности (рефрактерность проводящей системы сердца более продолжительна, нежели у типической мускулатуры).
Возбуждение при этом как бы пятится «задом наперед». На рис. 11 показаны процессы реполяризации желудочков, во время которых возникают векторы, чье направление совпадает с направлением во время деполяризации, но значительно меньшие по величине. Правило формирования результирующего вектора здесь такое же: мощность левого желудочка гораздо больше правого, поэтому преобладает положительный левый вектор, который дает устойчивый подъем пера вверх. Поскольку, длительность реполяризации желудочков больше, чем деполяризации, то продолжительность подъема пера тоже длительнее, нежели, чем при формировании R. В конце концов, при завершении реполяризации, положительный вектор исчезает, и перо возвращается на изолинию. Следует отметить, что сформированный зубец Т как правило положителен в тех отведениях, где положителен зубец R и отрицателен в отведениях типа QS – это правые грудные отведения по Вильсону и правые усиленные отведения от конечностей по Бейли.

Наконец, для завершения картины формирования нормальной ЭКГ, укажу на формирование последнего зубца U. Как уже было сказано, рефрактерность проводящей системы сердца более продолжительна, нежели у типической мускулатуры, поэтому реполяризация атипических кардиомиоцитов желудочков как бы запаздывает. Поэтому после завершения зубца T (особенно при низкой ЧСС), возникает дополнительный положительный вектор, быстро исчезающий после завершения реполяризации. Часто зубец U накладывается на Т, что проявляется расщеплением последнего, либо (чаще) ничем не проявляется. Завершение реполяризации миокарда желудочков составляет 5 фазу (рис. 12).

Итак, мы рассмотрели генез основных зубцов, сегментов и интервалов нормальной ЭКГ. Теперь, с учетом этих сведений рассмотрим механизм нарушений ЭКГ при ряде заболеваний.
При анализе ЭКГ электрокардиографическое заключение дается по определенной форме. Она включает в себя ряд пунктов:
1. Источник сердечного ритма. В норме такой источник – синусный узел, а сердечный ритм из синусного узла – синусный ритм. Диагностические критерии синусового ритма:
1) зубец Р синусного происхождения (везде положителен, кроме аVR);
2) постоянный и нормальный интервал PQ (0,12 – 0,18 с);
3) постоянная форма Р в каждом отведении.
2. Правильность или регулярность ритма. Критерий – постоянное расстояние Р-Р или R-R (для дифференциации физиологической синусовой аритмии – индекс Куна 0,2 – 0,25).
3. ЧСС – вычисляется делением 60 с на продолжительность одного сердечного цикла (R-R)
4. Положение электрической оси сердца – оценивается в трех плоскостях, для чего необходимо как минимум 12 отведений (3 стандартных, 3 усиленных от конечностей, 6 горизонтальных). Для оценки положения электрической оси сердца во фронтальной плоскости используется угол альфа – это угол между электрической осью, проведенной из середины треугольника Эйнтховена и осью первого стандартного отведения. У здоровых людей угол альфа колеблется от 0 до +90 град, причем от 20 до 70 град – нормальное положение электрической оси; от 20 до 0 – горизонтальное положение электрической оси; от 70 до 90 – вертикальное положение (варианты нормы). Если альфа больше 90 – отклонение вправо, если меньше 0 – отклонение влево, что указывает на патологические изменения. Определяется угол альфа либо с помощью построения треугольника Эйтховена, либо по номограммам и таблицам. Оценка положения электрической оси во фронтальной и сагиттальной плоскостях ведется по электрической позиции сердца (т.н. схема Вильсона). Для определения позиции исследуется сходство желудочковых комплексов в стандартных и усиленных отведениях от конечностей. Выделяют основную (среднюю), полугоризонтальную, горизонтальную, полувертикальную, вертикальную и неопределенную электрические позиции. При вертикальном положении сердца комплекс QRS в отведении aVL похож на комплекс QRS в отведениях V1 или V2. В отведении aVF он похож на V5-V6. При полувертикальном положении сердца комплекс QRS в отведении aVL имеет низкое напряжение, а в отведении aVF похож на комплекс QRS в V5,V6. При горизонтальном положении сердца комплекс QRS в отведении aVL похож на комплекс QRS в V5 или V6, а в отведении aVF – на V1 или V2. При полугоризонтальном положении сердца комплекс QRS в отведении aVL похож на комплекс QRS в отведениях V5,V6, а в отведении aVF имеет низкий вольтаж. При среднем положении сердца комплексы QRS в отведениях aVL и aVF похожи друг на друга и на V5, V6. Однако не всегда комплексы QRS в отведениях aVL и aVF имеют выраженную конфигурацию. В этих случаях говорят о т.н. неопределенном положении. Оценка положения электрической оси в горизонтальной плоскости ведется в помощью грудных отведений Вильсона по локализации т.н. переходной зоны (примерное равенство положительных и отрицательных зубцов желудочкового комплекса). В норме переходная зона находится в V3. Если переходная зона смещается в сторону правых грудных отведений, говорят о вращении электрической оси против часовой стрелки (поворот верхушкой вправо), если в сторону левых грудных отведений – говорят о вращении электрической оси по часовой стрелке (поворот верхушкой влево).
5. Последним пунктом электрокардиографического заключения является выявление электрокардиографической патологии в виде конкретного синдрома нарушений автоматизма, возбудимости и проводимости сердца.
Нарушения возбудимости сердечной мышцы чаще всего проявляются в возникновении активных эктопических очагов возбуждения в разных отделах сердца, что приводит к внеочередным сокращениям сердечной мышцы. Такие внеочередные сокращения носят название ЭКСТРАСИСТОЛИЙ. В зависимости от локализации патологического очага возбуждения различают предсердные, узловые, стволовые и желудочковые. Для экстрасистолии характерны два признака: интервал сцепления – фиксированное расстояние от предшествующего нормального желудочкового комплекса до появления внеочередного. Второй признак – компенсаторная пауза – выпадение очередного желудочкового комплекса из-за развившейся рефрактерности после экстрасистолы.
Итак, рассмотрим формирование патологической ЭКГ при желудочковой экстрасистолии (рис. 13). Предположим, в левом желудочке (где-то в проводящей системе левого желудочка) возникает эктопическая импульсация. Впишем оба желудочка в треугольник Энтховена и посмотрим формирование электрических векторов и их проекций на ось I стандартного отведения (левый желудочек) и III стандартном отведении (правый желудочек). Итак, в случае левожелудочковой экстрасистолы 1 фаза возбуждения начинается в левом желудочке и как обычно – это охват возбуждением межжелудочковой перегородки.
Вектор ЭМИ направлен слева направо и формируется зубец Q в I стандартном отведении и зубец R в III стандартном отведении. Левая половина межжелудочковой перегородки очень быстро возбуждается, а вот правая – очень медленно, ведь возбуждение идет из левого сердца. Поэтому в левом желудочке возбуждение выходит на волокна Пуркинье (образуя очень мощный левый вектор), что приводит к формированию в I отведении высокого R, а в III – умеренного S (происходит гашение отрицательного вектора продолжающимся довозбуждением межжелудочковой перегородки) – рис. 14.


В третью фазу идет доохват возбуждением основания левого желудочка (в I – S), в правом – доохват возбуждением только межжелудочковой перегородки. В четвертую фазу, когда в норме желудочки рефрактерны и регистрируется сегмент ST, в случае левожелудочковой экстрасистолы идет медленный (по типической мускулатуре) охват возбуждением правого желудочка. Какой же вектор при этом регистрируется – конечно, правый. Это приводит к появлению довольно глубокого и деформированного S в I отведении и такого же деформированного R в III стандартном отведении (рис. 15).

Рис. 15. Четвертая фаза возбуждения желудочков
при левожелудочковой экстрасистолии
Желудочковый комплекс как следствие, всегда уширен (больше 0,12 с) и деформирован. К моменту окончания 4 фазы в левом желудочке начинается обычная реполяризация – вектор реполяризации направлен от эпикарда к эндокарду – в I стандартном отведении формируется положительный Т. А вот в правом желудочке субэпикардиальные слои миокарда только что закончили возбуждение, а потому пребывают в рефрактерном состоянии. Поэтому, реполяризация начинается ретроградно – от субэндокардиальных отделов миокарда. Это приводит в к появлению выраженного отрицательного Т в III стандартном отведении (рис. 16).

Если посмотреть на сформированные ЭКГ, то хорошо видно, что признаком левожелудочковой экстрасистолы помимо деформации желудочкового комплекса, является и существенное отклонение электрической оси вправо – угол альфа больше 90 градусов (из-за длительного вектора доохвата возбуждением правого желудочка). Правожелудочковая экстрасистолия на ЭКГ выглядит с точностью, до наоборот – деформация желудочкового комплекса и отклонение электрической оси влево (меньше 0 градусов). Кстати, абсолютно сходные механизмы (и соответственно, сходные изменения ЭКГ) наблюдаются при блокадах ножек пучков Гиса, с той лишь разницей, что отсутствуют аритмия, интервал сцепления и компенсаторная пауза. Таким образом, знание механизмов формирования нормальной ЭКГ, дает ключ к пониманию развития патологических изменений ЭКГ и постановке правильного ЭКГ – заключения.
Проследим это утверждение на примере нарушения атриовентрикулярной проводимости. Последняя бывает 2-х форм – в виде поперечной (атриовентрикулярная блокада) и продольной (синдром Вольфа-Паркинсона-Уайта – WPW и синдром Лайона-Гононга-Левине – LGL) диссоциации. Синдром LGL является наиболее легким проявлением нарушения атриовентрикулярной проводимости – в виде уменьшения времени атриовентрикулярной задержки без деформации желудочкового комплекса (PQ < 0,12 с). Он связан с врожденным наличием дополнительного пучка Джеймса, шунтирующего узел Ашоффа-Тавара. Проявляется укорочением PQ. При наличии других шунтовых пучков (Кента, Махейма) возникает синдром WPW, имеющий более выраженные ЭКГ-проявления.
Рассмотрим механизм их появления (рис. 17). Предположим имеется добавочный путь проведения импульсов слева от атриовентирулярного узла (тип А синдрома WPW). При этом, возбуждение, охватив левое предсердие, не задерживаясь, идет на проводящую систему желудочков. Поэтому сегмент РQ резко укорочен, а иногда совсем не регистрируется. Зато дополнительный положительный вектор перехода возбуждения на ножку Гиса формирует т.н. дельта-волну, хорошо заметную в III стандартном отведении. Далее, выйдя на левую ножку Гиса, возбуждение формирует комплекс ЭКГ, сходный с левожелудочковой экстрасистолой (рис. 18). Действительно, довольно длительный охват возбуждением правой половины межжелудочковой перегородки, а затем и правого желудочка приводит к формированию в I стандартном отведении глубокого S, а в III стандартном – высокого и уширенного R (рис. 19). Электрическая ось ориентирована вправо, в грудных отведениях преобладают комплексы типа R (рис. 20).


Обратимся к электрокардиографическим проявлениям такой важной в клиническом отношении патологии сердца как ИБС с грозным осложнением в форме инфаркта миокарда. При инфаркте миокарда принято различать 3 зоны: зону некроза, зону повреждения вокруг нее и зону ишемии, расположенную снаружи от зоны повреждения. Ишемия миокарда сопровождается недостаточным снабжением сердца кислородом, что нарушает работу калий-натриевых насосов и из клетки выходит калий. Ишемия чаще поражает субэндокардиальную зону миокарда, что обусловлено более низким кровоснабжением по сравнению с субэпикардиальной зоной миокарда. На ЭКГ ишемия миокарда всегда затрагивает только зубец Т, в то время как желудочковый комплекс остается неизменным. Это связано с тем, что именно реполяризация (обусловленная ускоренным калиевым током) нарушается при ишемии.

Рассмотрим изменение зубца Т при субэндокардиальной ишемии (рис. 22). Предположим, имеется зона субэндокардиальной ишемии передней стенки левого желудочка. Возбуждение и левого и правого желудочка при этом не изменяются. Если посмотреть на проекции в координатах оси I стандартного отведения, то в 1 фазу формируется зубец Q (охват возбуждением межжелудочковой перегородки), во вторую фазу – зубец R (деполяризация миокарда желудочков), в 3 фазу – зубец S (охват возбуждением основания левого желудочка), в 4 фазу – сегмент S-T (рефрактерность кардиомиоцитов). Собственно изменения наблюдаются в 5 фазу – при формировании Т.

Если в норме возбуждение как бы исчезает со стороны эпикарда к эндокарду, то в случае субэндокардиальной ишемии, реполяризация левого желудочка задерживается в субэндокардиальном слое. Поэтому, если в правом желудочке вектор реполяризации уже исчез, то в левом он действует более длительно и это резко увеличивает размеры Т. Этот зубец становится остроконечным и симметричным, иногда по высоте превышая R – говорят о коронарном зубце T.
В случае же субэпикардиальной ишемии (рис. 21), эпикардиальные участки миокарда левого желудочка (в правом происходит все как обычно) позднее реполяризуются, нежели субэндокардиальные, поэтому реполяризация левого желудочка начинается от эндокарда. Вектор реполяризации при этом ориентирован вправо и формируется значительный отрицательный Т.
Повреждение миокарда, в отличие от ишемии сопровождается выраженными деструктивными изменениями – вакуолизацией, дистрофией мышечных волокон, нарушением структуры мембран. При этом из клетки начинает усиленно выходить калий и она интенсивно деполяризуется. Мембранный потенциал покоя начинает стремительно падать (достигая -5, -10 мв вместо «положенных» -90).
Проследим, как это отразится на ЭКГ (рис. 23). Предположим, имеется субэпикардиальное повреждение передней стенки левого желудочка. Возбуждение предсердий и узла Ашоффа-Тавара проходит как обычно, затем происходит охват возбуждением межжелудочковой перегородки – формируется обычный зубец Q – здесь тоже как обычно, превалирует отрицательный вектор. Далее, от эндокарда к эпикарду идут векторы возбуждения миокарда, причем левый вектор преобладает – формируется зубец R, однако он несколько снижен за счет того, что зона повреждения не деполяризуется как обычно (отрицательный заряд отсутствует). Однако, формирования нормального (изоэлектрического) сегмента ST не происходит потому, что зона повреждения заряжена положительно по отношению к возбужденному здоровому миокарду. Поэтому сохраняется дополнительный положительный вектор, который поднимает ST выше изолинии (элевация ST, симптом кошачьей спинки). Характерным для субэпикардиального повреждения является и снижение (депрессия) сегмента ТР, т.к. возникает другой вектор – из отрицательной зоны повреждения к положительному заряду остальной массы миокарда.

Рассмотрим ЭКГ-признаки некроза или собственно инфаркта миокарда. Участок некроза (также как и рубцовой ткани) в электрическом отношении представляет собой диэлектрик, блокирующие пров
Дата добавления: 2016-11-29; просмотров: 2519;










