Кристаллизация металлов
При переходе аморфного тела из жидкого состояния в твердое никаких качественных изменений в строении не происходит, что подтверждает монотонный ход кривой охлаждения (рис. 46, а). В твердом состоянии атомы в аморфном теле расположены так же хаотично, как и в жидком, но только более компактно и вследствие этого имеют более ограниченную свободу перемещения.
При нагреве всех кристаллических тел, в том числе металлов, всегда наблюдается четкая граница перехода из твердого состояия в жидкое. Такая же резкая граница существует и при переходе на жидкого состояния в твердое (рис. 46, б). 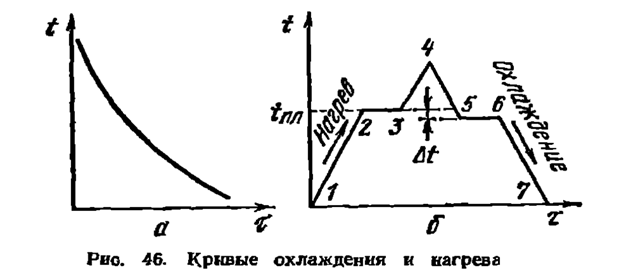
На участке кривой 1—2 (см. рис. 46, б) внешний подвод тепла сопровождается повышением температуры металла, сохраняющего спою кристаллическую решетку, атомы в которой увеличивают амплитуду колебания за счет поглощения тепловой энергии. На участке 2—3 подвод тепла продолжается, но он не приводит к повышению температуры, т. е. подводимая энергия целиком расходуется на разрушение кристаллической решетки и переход атомов в неупорядоченное состояние. Внешне это проявляется в переходе твердого состояния в жидкое. В точке 3 разрушаются последине участки кристаллической решетки, и продолжающийся подвод тепла вызывает повышение температуры жидкого металла (3—4).
При охлаждении наблюдается обратный процесс. На участке 5—6 происходит кристаллизация, сопровождающаяся выделением тепла, которое называется скрытой теплотой кристаллизации. Кристаллизация металла происходит не строго при температуре плавления, а при некотором переохлаждении ∆t, значение которого зависит от природы самого металла, от степени его загрязненности различными включениями и от скорости охлаждения. Чем меньше загрязнен металл включениями, тем больше степень переохлаждения при кристаллизации.
Образование кристаллической решетки сопровождается уменьшением запаса внутренней энергии тела.
Согласно второму закону термодинамики, всякая система стремится к минимальному значению свободной энергии F=U—TS. где F — свободная энергия; U — внутренняя энергия системы; Т — абсолютная температура; S — энтропия. Изменение свободной энергии в зависимости от температуры для твердого и жидкого состояний схематически показано на рис. 47.

При температуре Тпл свободные энергии обоих состояний равны. Такую температуру называют равновесной или теоретической температурой кристаллизации.
Как было отмечено, ни плавление, ни кристаллизация не происходят точно при этой температуре. Например, для начала кристаллизации необходимо переохлаждение до Т1.
Разность между теоретической и фактической температурами кристаллизации называется степенью переохлаждения ∆Т=Тил—Т1.
Законы кристаллизации
Механизм кристаллизации металла состоит в том, что при соответствующем понижении температуры внутри тигля с жидким металлом начинают образовываться мелкие кристаллики, называемые центрами кристаллизации или зародышами.
Для начала роста кристаллов из жидкого металла вокруг возникающих центров кристаллизации необходимо, чтобы свободная энергия металла уменьшилась. Если же в результате образования зародыша свободная энергия металла увеличивается, то зародыш растворяется. Минимальный размер способного к росту зародыша называется критическим размером зародыша, а такой зародыш — устойчивым.
Чем больше степень переохлаждения, понижающая свободную энергию металла, тем меньше критический размер зародыша.
Вокруг образовавшихся центров начинают расти кристаллы (рис. 48). По мере роста кристаллов в металле, оставшемся еще в жидком состоянии, продолжают возникать новые центры кристаллизации. Каждый из растущих новых кристаллов ориентирован в пространстве произвольно. Как видно из схемы, поверхности растущих кристаллов соприкасаются, их правильная внешняя форма нарушается, получается произвольной.
Кристаллы с неправильной внешней формой называются зернами или кристаллами. Твердые тела, в том числе и металлы, состоящие из большого количества зерен, называют поликристаллическими.

Как установлено Д. К. Черновым, процесс кристаллизации состоит из двух элементарных процессов: зарождения центров кристаллизации и роста кристаллов из этих центров. Гораздо позже Тамман, изучая процесс кристаллизации, установил зависимость числа центров кристаллизации (ч. ц.) и скорости роста кристаллов (с. р.) от степени переохлаждения ДТ (рис. 49).
Размер образовавшихся кристаллов зависит от степени переохлаждения.
1. Какое основное отличие перехода из твердого состояния в жидкое аморфных и кристаллических тел
2. Что такое равновесная температура
3. Как называется разница между фактической температурой кристаллизации и теоретической температурой кристаллизации
4. Опешите механизм кристаллизации жидкого металла
5. Объясните почему при постоянном подводе тепла на участке 2-3 нет увеличения температуры

Дата добавления: 2016-11-26; просмотров: 1967;










