Классификация органических реакций
Все химические реакции сопровождаются разрывом одних связей и возникновением других. Органические реакции подчиняются, в принципе, тем же законам, что и реакции неорганических веществ, но имеют свои особенности. Так в отличие от последних, в которых обычно участвуют ионы, в органических реакциях чаще всего принимают участие молекулы. Такие реакции протекают гораздо медленнее и для их ускорения часто используют катализаторы или создают соответствующие условия (повышают температуру или давление). При этом выход конечного продукта обычно невысок (50-80%), но и это удовлетворяет химиков-органиков, так как в процессе его получения идет не одна реакция, а несколько, которые называют побочными. Поэтому органическую реакцию записывают не в виде химического уравнения (с приведением стехиометрических соотношений реагирующих веществ), а ее схему, которая показывает только исходные вещества и основной продукт реакции, а также условия проведения реакции. В этом случае вместо знака равенства (=) используют стрелку (→), указывающую направление превращения веществ. Часто запись уравнения реакции изображают в сокращенном виде: над стрелкой указывают условия проведения реакции, а под стрелкой – побочные вещества, которые выделяются в реакции (со знаком минус).
Все органические реакции классифицируют:
1. По характеру химических превращений органические реакции делят на следующие типы.
Реакция замещения. Один атом (или группа атомов) замещается на другой атом (или группу атомов) с образованием новой молекулы:
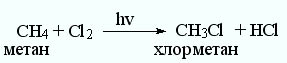
Реакция присоединения. В этом случае из двух (или нескольких) молекул образуется одно новое вещество:

К реакции присоединения можно отнести реакцию восстановления (действие восстанавливающего реагента обозначают символом [Н]):

Реакция восстановления противоположна реакции окисления. Частным случаем реакции восстановления является гидрирование:

Реакция отщепления. В результате этой реакции образуется новое вещество, содержащее кратную связь:

Перегруппировка. Такие реакции приводят к внутримолекулярным перемещениям атомов или групп атомов без изменения молекулярной формулы веществ, участвующих в реакциях:

Окисление – реакция, при которой под действием окисляющего реагента (его обозначают символом [O]) образуется новое соединение:

Реакции конденсации и поликонденсации являются также частным случаем реакции присоединения. В результате соединения нескольких молекул друг с другом, сопровождающегося выделением простых веществ (H2O, NН3 и др.), образуется сложное вещество с более высокой молекулярной массой:

Реакция разложения (расщепления) приводит к образованию новых веществ более простого строения:

2. По механизмам их протекания и характеру реагента, действующего на молекулу.
Дата добавления: 2016-11-04; просмотров: 2222;










