УСТРОЙСТВО И ПРИНЦИП РАБОТЫ СПЕКТРОГРАФА
Спектральные методы исследования находят в настоящее время широкое применение в лабораторной практике. Свет представляет собой совокупность электромагнитных волн очень высокой частоты. Если на его пути поставить призму, то лучи будут преломляться под разными углами
(дисперсия), и дают спектры. Различают спектры по происхождению (атомные, молекулярные) по способу получения (испускания, поглощения), по виду (сплошной, линейчатый, полосатый).
I.Атомные спектры.
Состояние электрона в атоме характеризуется волновой функцией, которая содержит безразмерные величины - квантовые числа. Квантовые числа могут принимать ряд целочисленных значений. Этими числами задается атомная орбиталь, распределение электронов по атомным орбиталям и определяется электронная конфигурация атома.
Основным состоянием атомной системы является состояние с наименьшей энергией.
Возбужденным состоянием атомной системы называют состояние, в котором полная энергия больше энергии основного состояния. Энергия электронов атома тоже зависит от квантовых чисел и может принимать только строго определенные значения энергии Е, которые называются энергетическими уровнями. Для одноэлектронного атома энергетические уровни атома и электрона совпадают.
Поглощение и испускание энергии атома связано с квантовыми переходами электронов с одного уровня на другой.
Различаются два типа переходов:
I- с излучением или поглощением энергии квантов.
II.-без излучения или поглощения электромагнитной энергии.
Излучаемая атомами энергия составляет спектр излучения, поглощаемая- спектр поглощения.
Квантовые переходы не могут происходить между любыми уровнями.
Существуют правила отбора или запрета, формирующие условия, при которых переходы возможны или невозможны (маловероятны).
В атомах в результате взаимодействия электронов между собой картина энергетических уровней усложняются. Энергия атома в целом определяется заданием квантовых чисел: n – главнее квантовое число, определяет уровни энергии электрона и L - орбитальное квантовое число, характеризует орбитальный момент электрона относительно ядра. Совокупность квантовых чисел n и L и определяет электронную конфигурацию атома. Как правило, каждой конфигурации принадлежит набор энергетических уровней.
При переходе между уровнями излучается или поглощается квант электромагнитной энергии, частота которого определяется формулой Планка: hv=Е2-Е1
II.Молекулярные спектры 
Молекулярные спектры значительно сложнее атомных. Рассмотрим энергетические уровни простейшей двухатомной молекулы. Каждому электронному состоянию соответствует своя система колебательных уровней Viодно из которых основное и несколько возбужденных. Каждому колебательному уровню Vi соответствует своя система вращательных подуровней Ii.
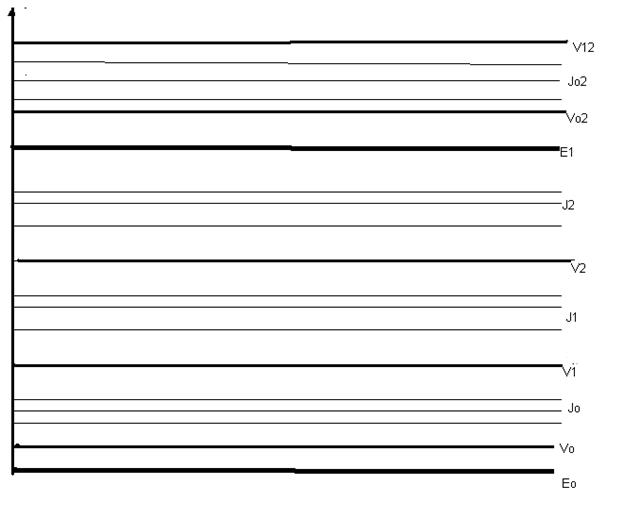
Рис.1 Энергетические уровни молекул
Чисто вращательные молекулярные спектры дают вещества в газообразном состоянии, чисто колебательные, а тем более чисто электронные спектры молекул получить нельзя, т.к. изменяется все три вида движения молекул. Колебательно-вращательные спектры можно получить при любом агрегатном состоянии.
В возбужденном состоянии молекула резко отличается по своим свойствам и строению, по сравнению с основным состоянием.
Дата добавления: 2020-12-11; просмотров: 159;










