Открытие и разработка системы изотопов, в особенности открытие закона сдвига
В1913 г Ф. Содди и К.Фаянс сформулировали правило смещения, позволяющее предсказать место в периодической системе элемента — продукта радиоактивного распада.

Фредерик Содди (1877 - 1956) - английский радиохимик, член Лондонского королевского общества (1910), лауреат Нобелевской премии по химии (1921). Совместно с Резерфордом предложил теорию радиоактивного распада, послужившую началом развития современного учения об атоме и атомной энергии. В 1903 Резерфорд и Содди установили, что радиоактивный распад протекает по закону, описывающему ход мономолекулярной реакции. Рамзай и Содди спектроскопическим путём обнаружили образование гелия из радона. в 1913 Содди и К.Фаянс сформулировали правило смещения. Экспериментально доказал (1915), что радий образуется из урана.

Казимир Фаянс (1887 –1975) - американский физико-химик. Поляк по происхождению. Одновременно с Ф.Содди установил (1913) правило смещения при распаде радиоактивных элементов; совместно с Ф.Панетом сформулировал (1913) правило соосаждения радиоактивных элементов (правило Фаянса — Панета). Основные труды Фаянса в области физической химии посвящены рефрактометрическим исследованиям, изучению связи деформации электронных оболочек с химическими и оптическими свойствами неорганических соединений, изучению недиссоциированных молекул и комплексных ионов в растворах сильных электролитов.
Правило сдвига, или правила смещения: при альфа-распаде химическая природа элемента изменяется так, что он смещается на две клетки влево по периодической системе, при бета-распаде – на одну клетку вправо. Правило четко увязало структуру трех радиоактивных семейств с таблицей Менделеева. Позднее было доказано, что родоначальники семейств – долгоживущие радиоактивные изотопы торий-232, уран-238 и уран-235.
3.Открытие закона Г. Мозли
В 1895 году В. Рентген открыл рентгеновские лучи. За открытием Рентгена последовали эксперименты других исследователей, обнаруживших много новых свойств и возможностей применения этого излучения.
Одним из них был Г. Мозли, установивший в 1913 г зависимость между длиной волны излучения и атомным номером элемента.

Генри Гвин Джефрис Мозли (1887 - 1915) - английский физик, один из основоположников рентгеновской спектроскопии. В 1913 в серии блестящих экспериментов установил зависимость между частотой спектральных линий характеристического рентгеновского излучения и атомным номером излучающего элемента. В 1913 г. создал и представил исторически первый радиоизотопный источник электрической энергии (атомную батарею Beta Cell). В 1914 Мозли опубликовал работу, в которой сделал вывод, что между элементами алюминием и золотом в периодической таблице должно находиться три (как оказалось позже, четыре) элемента.
Г. Мозли установил, что длина волны рентгеновского излучения своя у каждого элемента. Она увеличивается с возрастанием атомной массы. Г. Мозли связал частоту этого излучения с порядковым номером элемента. Закон Мозли подтвердил, что изменение порядковых номеров элементов в периодической системе соответствовало последовательному увеличению зарядов ядер их атомов.
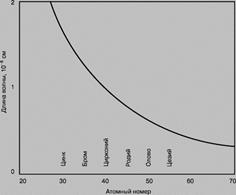
Длина волны характеристического рентгеновского излучения, испускаемого химическими элементами, зависит от атомного номера элемента. Кривая соответствует закону Мозли: чем больше атомный номер элемента, тем меньше длина волны характеристической линии.
В связи с новыми открытиями периодический закон принял следующую современную формулировку:
Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядра атома (порядкового номера элемента).
Почему же свойства элементов и его соединений изменяются периодически? В чем причина периодичности?
Ответ на данный вопрос также позволяет дать теория строения атома. Величина заряда ядра - главная характеристика элемента, мера его индивидуальности. От Z элемента зависят все остальные его свойства, он определяет число электронов и их состояние в атоме.
Возрастание Z атомов элементов от 1 до 107 приводит к периодическому повторению электронных структур атомов и числа электронов на внешнем энергетическом уровне. В этом - физический смысл периодического закона и причина периодичности изменения свойств элементов.
Дата добавления: 2016-05-30; просмотров: 1388;










