Физика явления. Рентгеновские лучи
Рентгеновские лучи – это электромагнитное излучение, которое возникает либо при торможении свободно движущейся заряженной частицы, либо при электронных переходах во внутренних оболочках атома. Спектры этих двух видов излучения существенно различаются. В первом случае это тормозной спектр с непрерывным распределением по длинам волн, коротковолновая граница которого обрывается при энергии, равной максимальной кинетической энергии заряженной частицы. Строение тормозного спектра не зависит от материала, на котором происходит торможение заряженной частицы (в рентгеновской трубке это материал анода).
Во втором случае спектр линейчатый. Он зависит от материала, излучающего его, и характеризуется им. Каждый элемент обладает своим, характерным для него линейчатым спектром, поэтому линейчатые рентгеновские спектры называются также характеристическими.
Рентгеновское излучение лежит в диапазоне длин волн примерно от 102 до 10–2 Å, что по энергии фотонов соответствует области от 100 эВ до 1 МэВ. Однако четких границ здесь нет; так, фотоны в синхротронном излучении (тормозном спектре) могут обладать энергией, большей 1 МэВ. Рентгеновский диапазон обычно делится на две части, l < 2Å соответствует жесткому излучению, а l > 2Å – мягкому.
Рентгеновские лучи обладают проникающей способностью, тем более сильной, чем жестче они (чем короче их длина волны). Это свойство послужило причиной широкого использования рентгеновского излучения в различных аппаратах, – от рентгеновского томографа в медицине до приборов количественного элементного анализа высокой точности.
Предлагаемая лабораторная задача посвящена изучению характеристических спектров излучения (эмиссии) различных элементов, поэтому здесь будет кратко описано явление возникновения этих спектров и их свойства.
В нормальном состоянии многоэлектронный атом представляет собой положительно заряженное ядро, окруженное системой электронных оболочек от самой внутренней с главным квантовым числом n=1, до внешней с n, соответствующим данному элементу (максимальное значение n=7 соответствует концу таблицы периодической системы элементов). Оболочки обозначаются буквами K,L,M,N,O,P,Q в соответствии с ростом n, начиная от единицы. На каждой оболочке находится определенное число электронов в соответствии с принципом Паули. Следует отметить, что понятие “оболочка” более соответствует энергетическому понятию (которое можно заменить термином “уровень энергии”), чем координатному. В соответствии с квантовой механикой электроны в атоме как бы “размазаны” по объему с максимумом вероятности локализации на оболочке. В то же время в энергетическом пространстве наблюдается более четкое разделение между оболочками - уровнями энергии, хотя и здесь наблюдается определенное их перекрывание.
В нормальном состоянии атом не излучает и не поглощает энергию. Излучение, связанное с переходами во внутренних оболочках возможно лишь в случае, когда один или несколько внутренних электронов будут удалены. Любой электрон, принадлежащий внешней (по отношению к образовавшейся вакансии – “дырке”) оболочке, оказывается возбужденным. Это приводит к переходам с более высоких уровней на уровень вакансии с излучением рентгеновского кванта.
Если выбит K-электрон, то переходы на образовавшуюся вакансию с выше лежащих L,M,N... уровней образуют наиболее коротковолновую K- серию излучения. Аналогичный процесс наблюдается при переходах на вакансии L-уровней (L-серии), вакансии M-уровней (M-серии) и т.д.
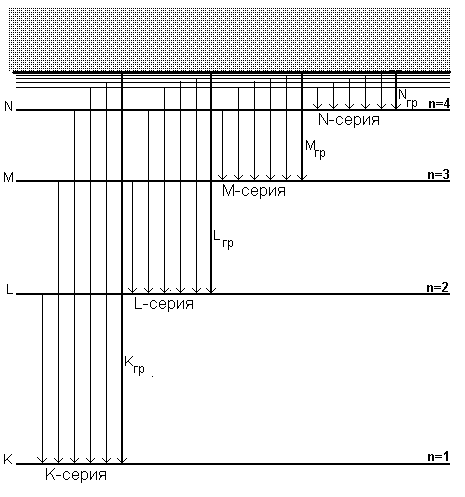
Рис 1. Схема рентгеновских уровней и переходов, образующих K, L, M, N серии. Kгр, Lгр, Mгр, Nгр - границы серий, соответствующие переходам в непрерывный спектр. n - главное квантовое число.
Разность энергий конечного (  ) и начального (
) и начального (  ) уровней равна энергии Е = hn = ç
) уровней равна энергии Е = hn = ç  -
-  ç фотона, испускаемого при переходе из начального i-го в конечное f-е состояние и соответствует спектральной линии частоты n.
ç фотона, испускаемого при переходе из начального i-го в конечное f-е состояние и соответствует спектральной линии частоты n.
Внутренний электрон атома находится в экранированном кулоновском поле и его состояние очень похоже на состояние электрона водородоподобного иона. Разница состоит в том, что находится он не в поле с зарядом Ze, а в поле с эффективным зарядом Zэфe=(Z – a1)e, где a1 - постоянная полного экранирования.
Выражение для энергии внутреннего электрона может быть представлено формулой, подобной формуле для атома водорода, но с эффективным зарядом (Z – a1) e.
 . (1)
. (1)
Энергия фотона излучения, соответствующая переходу этого электрона в нижнее вакантное состояние, равна
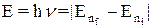 =
= 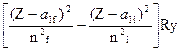 (2)
(2)
Здесь Ry = 13,6 эВ (Ридберг) - величина, равная потенциалу ионизации атома водорода, a1f и a1i - постоянные полного экранирования конечного состояния f и начального i, nf и ni -соответствующие главные квантовые числа.
Как отмечалось выше, согласно квантовой механике, электрон в состоянии с квантовым числом n можно с большой степенью вероятности найти, на характерном для данного n расстоянии rn от ядра (т.е. в пределах слоя, определяемого нами как оболочка). Однако существует конечная вероятность обнаружить его как внутри, так снаружи оболочки. Это приводит к тому, что в формировании постоянной a1 принимают участие все электроны атома. Теоретическое вычисление a1 представляет сложную задачу, и обычно для ее определения используют экспериментальные данные.
Постоянные a1i,f - зависят от главного квантового числа n и орбитального квантового числа l.
Так, например, в церии (Z=58) для K оболочки (n=1) a1K=3,5; а для L оболочки (n=2) a1L=15,5. Наблюдается также незначительный рост этой величины с увеличением Z.
Несмотря на то, что a1i,f существенно зависит от n, разность в формуле (2)
 (3)
(3)
можно заменить на
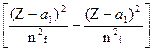 (4)
(4)
где постоянные экранирования a1 одинаковы и не равны a1i,f. Подчеркнем, что a1 имеет смысл некой условной средней постоянной экранирования. Эта величина также зависит от n, l и Z. Так для 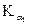 линий элементов с атомными номерами 20 < Z < 30 значение a1 = 1,13, а для
линий элементов с атомными номерами 20 < Z < 30 значение a1 = 1,13, а для 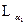 линий и Z ³ 62: a1 = 7,9.
линий и Z ³ 62: a1 = 7,9.
Проведенное преобразование приводит выражение (2) к виду
Е=hn=(Z-a1)2Ry(  ), (5)
), (5)
которое в форме
 (6)
(6)
или
 (7)
(7)
известно как Закон Мозли.
В формуле (7) k - волновое число ( k = 1/l), R - постоянная Ридберга (R=1,09678×105 см-1). Выражения (6) и (7) демонстрируют линейную зависимость квадратного корня из энергии фотона от атомного номера Z.
Из выражения (1) видно, что закону Мозли подчиняется также и энергия уровня. Следует подчеркнуть, что закон Мозли не точный. Отклонения от линейности наблюдаются с ростом Z и длины волны рентгеновского излучения.

Рис. 2 Диаграммы Мозли для K и L серий.
Дата добавления: 2020-07-18; просмотров: 159;










