Термохимия. Закон Гесса
Термохимия – это раздел химической термодинамики, в котором изучают тепловые эффекты химических реакций и устанавливают их зависимости от различных физико-химических параметров. В задачу термохимии также входит измерение теплоёмкостей веществ, теплот фазовых переходов, теплот образования и разбавления растворов. Данные, полученные в термохимии, используют в теоретической химии и применяют в практике для расчёта аппаратуры, теплового баланса, оптимального режима процесса при создании новых видов топлива.
Тепловой эффект химической реакции – это теплота, выделяемая или поглощаемая в результате реакции при соблюдении следующих условий:
1.давление Р или объём V системы постоянны;
2.не совершается никакой другой работы, кроме работы расширения;
3.температура исходных веществ и продуктов реакции одинакова.
Термохимические уравнения –это уравнения реакций, в которых указаны тепловые эффекты данных реакций. В термохимии выделяют экзотермические и эндотермические реакции. Экзотермические реакции – это реакции, идущие с выделением тепла. Эндотермические реакции – это реакции, идущие с поглощением тепла.
Например, экзотермическая реакция:
H2(г.) + Cl2(г.) ® 2HCl(г.) + 184,8 кДж (количество теплоты QP);
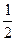 H2(г.) +
H2(г.) + 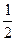 Cl2(г.) ® HCl(г.); DrH°298 = –92,4
Cl2(г.) ® HCl(г.); DrH°298 = –92,4 
(DrH° – мольный тепловой эффект при постоянном Р).
Индекс «r» в обозначении теплового эффекта от англ. reaction – реакция. Индекс «°» означает, что данная термодинамическая величина относятся к стандартному состоянию чистого вещества. За стандартное состояние чистого жидкого или твёрдого (кристаллического) вещества принимают его наиболее устойчивое физическое состояние при данной температуре Т и давлении Р = 1 атм (760 мм рт. ст., 101325 Па).
За стандартное состояние чистого газа принимают воображаемое состояние, при котором газ, находясь при данной Т и Р = 1 атм, подчиняется законам идеальных газов, а его энтальпия равна энтальпии реального газа.
За стандартное состояние раствора принимают воображаемое состояние, при котором раствор, находясь при данной Т, Р = 1 атм и концентрации С = 1 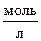 , обладает свойствами бесконечно разбавленного раствора. В биохимии для стандартного состояния раствора принято использовать концентрацию ионов H+, равную 10–7
, обладает свойствами бесконечно разбавленного раствора. В биохимии для стандартного состояния раствора принято использовать концентрацию ионов H+, равную 10–7 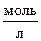 .
.
В 1984 г. ИЮПАК рекомендовал использовать в качестве давления стандартного состояния вещества 105 Па (1 бар) вместо традиционной 1 атм (IUPAC – по первым буквам англ. International Union of Pure and Applied Chemistry – Международный союз теоретической и прикладной химии).
Количество теплоты QP и мольный тепловой эффект DrH связаны соотношением:
 . .
| (2.13) |
где n – количество реагента или продукта реакции, моль.
Пример 2.2. При соединении 2,1 г железа с серой выделилось 3,77 кДж теплоты. Рассчитайте мольный тепловой эффект DrH реакции образования сульфида железа.
Решение:
Fe(a-кр.) + S(ромб.) ® FeS(a-кр.).
Из формулы (1.1) выразим количество железа:
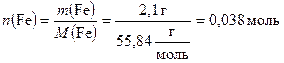 .
.
По формуле (2.13) рассчитаем мольный тепловой эффект:
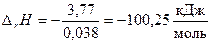 .
.
Стандартный мольный тепловой эффект DrH°298 = –100,42  [Равдель];
[Равдель];
отклонение 0,2 %.
Ответ: DrH = –100,25  .
.
Теплоёмкость тела(системы тел) – это отношение количества теплоты, подведённой или отведённой в данном процессе, к изменению температуры, которое при этом происходит. Физический смысл теплоёмкости заключается в следующем. Теплоёмкость численно равна количеству теплоты, которое необходимо подвести к системе, чтобы повысить её температуру на 1 К при условиях:
1.в системе отсутствуют химические реакции и фазовые переходы,
2.из всех видов работ система может совершать только работу расширения PDV.
В СИ теплоёмкость выражается в 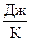 . Обычно С относят к 1 кг вещества (удельная теплоёмкость,
. Обычно С относят к 1 кг вещества (удельная теплоёмкость, 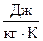 ) или к 1 моль вещества (мольная теплоёмкость,
) или к 1 моль вещества (мольная теплоёмкость, 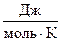 ). При физико-химических и термодинамических расчётах пользуются, как правило, мольными теплоёмкостями.
). При физико-химических и термодинамических расчётах пользуются, как правило, мольными теплоёмкостями.
Различают истинную и среднюю теплоёмкость. Истинная мольная теплоёмкость– это отношение бесконечно малого количества теплоты, которое нужно подвести к 1 моль вещества, к бесконечно малому приращению температуры, которое при этом наблюдается. Для изохорного и изобарного процессов истинные мольные теплоёмкости равны соответственно:
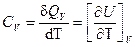 , ,
| (2.14) | |
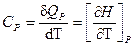 . .
| (2.15) |
Средняя мольная теплоёмкость 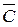 в интервале температур от Т1 до Т2 – отношение конечного количества теплоты, подведённого к 1 моль вещества, к разности температур
в интервале температур от Т1 до Т2 – отношение конечного количества теплоты, подведённого к 1 моль вещества, к разности температур 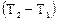 . Для изохорного и изобарного процессов средние мольные теплоёмкости равны соответственно:
. Для изохорного и изобарного процессов средние мольные теплоёмкости равны соответственно:
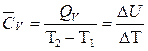 , ,
| (2.16) | |
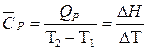 . .
| (2.17) |
В термодинамические выражения обычно входит истинная теплоёмкость, для приближённых расчётов используют среднюю теплоёмкость.
Пример 2.3. В сообщающемся с атмосферой стеклянном сосуде смешали 40 см3 раствора HNO3 (концентрация С = 2 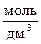 ) и 40 см3 раствора KOH (С = 2
) и 40 см3 раствора KOH (С = 2 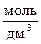 ). В результате реакции нейтрализации сильной кислоты сильным основанием температура системы повысилась на 9 К. Рассчитайте мольный тепловой эффект реакции нейтрализации DrH, если удельные средние теплоёмкости водного раствора и стекла составляют соответственно:
). В результате реакции нейтрализации сильной кислоты сильным основанием температура системы повысилась на 9 К. Рассчитайте мольный тепловой эффект реакции нейтрализации DrH, если удельные средние теплоёмкости водного раствора и стекла составляют соответственно: 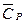 (р.) = 4,18
(р.) = 4,18 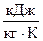 ,
, 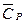 (ст.)= 0,75
(ст.)= 0,75 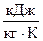 ; масса стеклянного сосуда m(ст.) = 223 г; плотность раствора r(р.) =1
; масса стеклянного сосуда m(ст.) = 223 г; плотность раствора r(р.) =1  . Потерями тепла в окружающую среду пренебречь.
. Потерями тепла в окружающую среду пренебречь.
Решение:
HNO3(р.) + KOH(р.) ® KNO3(р.) + H2O(ж.);
H+ + NO3– + K+ + OH– ® K+ + NO3– + H2O;
H+ + OH– ® H2O.
Из формулы (2.17) количество теплоты QP, выделившейся в ходе реакции нейтрализации:
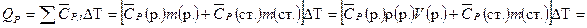
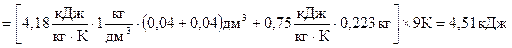 .
.
Количество прореагировавшей кислоты (или основания):
n = VC = 0,04 дм3 × 2 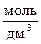 = 0,08 моль.
= 0,08 моль.
По формуле (2.13) мольный тепловой эффект реакции:
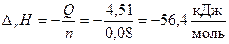 .
.
Стандартный мольный тепловой эффект DrH°298 = –55,8  [Равдель];
[Равдель];
отклонение 1,1 %.
Ответ: DrH = –56,4  .
.
Основным законом термохимии является закон Гесса, сформулированный в 1840 г. Г.И. Гессом:
Тепловой эффект химических реакций зависит только от природы и состояния исходных веществ и конечных продуктов, но не зависит от способа перехода от исходного состояния к конечному.
Закон Гесса вполне строго выполняется только для изохорных процессов (когда тепловой эффект QV в соответствии с (2.5) равен DU) и изобарных процессов (когда QP в соответствии с (2.6) равен DН). Хотя закон Гесса был установлен раньше, чем введено 1-ое начало термодинамики, однако его можно рассматривать как вывод из 1-го начала термодинамики при условии изохорного или изобарного процессов.
Рассмотри закон Гесса на примере реакции окисления углерода до СО2(г.) (рис. 2.1). В качестве исходных веществ возьмём кислород и уголь (считая его чистым углеродом в аллотропной модификации графит), а в качестве конечного продукта – СО2(г.). Переход от исходных веществ к конечному продукту можно осуществить, непосредственно сжигая уголь до СО2 (тепловой эффект реакции DrН1). Но можно также провести процесс в две стадии, получая в первой из них СО (тепловой эффект DrН2) и сжигая затем СО во второй стадии до СО2 (тепловой эффект DrН3). Такой двухстадийный процесс реализуется, например, в газогенераторном двигателе, где горючее сгорает в генераторе до СО, а уже СО сгорает до СО2 в цилиндре мотора. Закон Гесса позволяет связать тепловые эффекты этих трёх процессов простым уравнением:
| DrН1 = DrН2 + DrН3. | (2.18) |
Пользуясь уравнением (2.18), легко рассчитать любой из тепловых эффектов, если известны все остальные. В нашем случае экспериментально (методом калориметрии) можно измерить DrН1 и DrН3, однако сгорание С до СО при невысоких температурах затруднительно, т. к. кроме СО образуется СО2. Поэтому возможность определить тепловой эффект DrН2 расчётным путём является весьма ценной. Итак, мольные тепловые эффекты реакций:
| С(графит) + О2(г.) ® СО2(г.), | DrН°1 = –393,51  ; ;
|
СО(г.) + 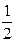 О2(г.) ® СО2(г.), О2(г.) ® СО2(г.),
| DrН°3 = –282,98  ; ;
|
С(графит) + 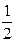 О2(г.) ® СО(г.), О2(г.) ® СО(г.),
| DrН°2 = ? |
Согласно уравнению (2.18):
DrН°2 = DrН°1 – DrН°3 = –393,51 – (–282,98) = –110,53  .
.
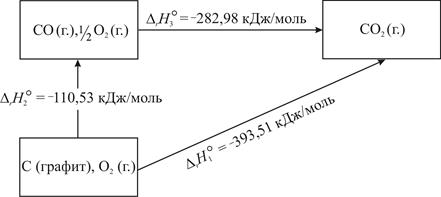
| Рис. 2.1.Схема, иллюстрирующая закон Гесса на примере реакции окисления углерода до СО2 [Равдель] |
Важное практическое значение закона Гесса заключается в том, что он даёт возможность вычислить тепловые эффекты химических реакций, для которых они не могут быть экспериментально измерены в требуемых условиях, или, когда процессы ещё не осуществлялись. Кроме того, закон Гесса применяется не только к химическим реакциям, но и к процессам растворения, испарения, кристаллизации, адсорбции и др. При расчёте тепловых эффектов различных химических реакций с использованием закона Гесса особое значение имеют два вида тепловых эффектов: теплота образования и теплота сгорания.
Теплота образования(стандартная энтальпия образования) –это теплота образования 1 моль данного соединения из простых веществ, отвечающих наиболее устойчивому состоянию рассматриваемого элемента при данной температуре и атмосферном давлении (101325 Па). Она обозначается DfН°T (индекс «f» от англ. formation – образование). В справочниках значения DfН°T приводятся для Т = 298,15 К (обозначаются DfН°298). Например: теплота образования 1 моль кристаллического сульфита натрия Na2SO3 равна тепловому эффекту реакции образования 1 моль сульфита натрия в данной его кристаллической модификации из металлического натрия, серы (в ромбической модификации) и газообразного кислорода:
2Na(кр.) + S(ромб.) + 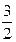 О2(г.) ® Na2SО3(кр.), О2(г.) ® Na2SО3(кр.),
| DfН°298(Na2SО3(кр.)) =
= –1089,43  . .
|
Теплоты образования простых веществ в термодинамически устойчивом состоянии (например: H2(г.), Cl2(г.), O2(г.), С(графит), S(ромб.)) для стандартного состояния чистого вещества принимаются равными нулю.
Теплота сгорания (стандартная энтальпия сгорания)– это тепловой эффект реакции окисления кислородом 1 моль вещества с образованием высших оксидов при данной температуре и атмосферном давлении (обозначается DсН°T). В справочниках значения DсН°T приводятся для Т = 298,15 К (обозначаются DсН°298, индекс «с» от англ. combustion – сгорание). Если получаются другие продукты сгорания, это специально оговаривается. В качестве продуктов сгорания элементов С, Н, N, S принимаются соответственно СО2(г.), Н2О(ж.), N2(г.), SO2(г.). Например: теплота сгорания жидкого нитробензола C6H5O2N:
C6H5O2N(ж.) + 6 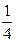 О2(г.) ® 6СО2(г.) + 2 О2(г.) ® 6СО2(г.) + 2 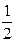 Н2О(ж.) + Н2О(ж.) + 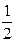 N2(г.), N2(г.),
| DсН°298(C6H5O2N(ж.)) =
= –3091,2  . .
|
Теплоты сгорания продуктов сгорания, а также кислорода O2(г.) для стандартного состояния чистого вещества принимаются равными нулю.
Из закона Гесса вытекает ряд следствий, два из которых наиболее широко используются при вычислении тепловых эффектов реакций.
Первое следствие:тепловой эффект реакции DrН°T равен разности между суммами теплот образования продуктов реакции и исходных веществ, взятых с коэффициентами, равными стехиометрическим.
Обратимся к произвольной изобарной реакции вида:
| aA +bB ® cC + dD. | (2.19) |
Тепловой эффект при температуре Т (DrН°T) для данной реакции:
| DrН°T= [cDfН°T(C) + dDfН°T(D)] – [aDfН°T(A) + bDfН°T(B)] | (2.20) |
или в общем случае:
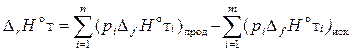 , ,
| (2.21) |
где pi – стехиометрические коэффициенты соответствующих веществ в уравнении реакции.
Пример 2.4. Рассчитайте тепловой эффект реакции при Т = 298,15 К и Р = 1 атм DrН°298, пользуясь данными по теплотам образования веществ – участников реакции:
CaC2(a-кр.) + 2H2O(ж.) ® Ca(OH)2(кр.) + C2H2(г.).
Решение:
Теплоты образования DfН°298 веществ – участников реакции [Равдель]:
| Вещество | CaC2(a-кр.) | H2O(ж.) | Ca(OH)2(кр.) | C2H2(г.) |
DfН°298, 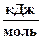
| –59,83 | –285,83 | –985,12 | 226,75 |
По 1-му следствию из закона Гесса (2.20):
DrН°298 = [DfН°298(Ca(OH)2(кр.)) + DfН°298(C2H2(г.))] – [DfН°298(CaC2(a-кр.)) +
+ 2DfН°298(H2O(ж.))] = [–985,12 + 226,75] – [–59,83 + 2×(–285,83)] = –127,88 кДж.
Данная реакция является экзотермической, протекает с выделением теплоты.
Ответ: DrН°298 = –127,88 кДж.
По 1-му следствию из закона Гесса можно вычислить не только тепловые эффекты для большого числа химических реакций, но и теплоты фазовых переходов и других физико-химических процессов. Фазовый переход можно записать в общем виде: Фаза(1) ® Фаза(2), а теплоту фазового перехода при данной температуре и атмосферном давлении: DtrН°T. Индекс «tr» от англ. transition – переход. Например, для фазовых переходов первого рода: при плавлении – теплота плавления DmН («m» от англ. melting – плавление), при испарении – теплота испарения DvН («v» от англ. vaporization – испарение), при сублимации – теплота сублимации DsН («s» от англ. sublimation – сублимация). DtrН°T можно рассчитать по формуле (2.21).
Пример 2.5. Рассчитайте теплоту испарения DvН°298 H2O(ж.) ® H2O(г.) по 1-му следствию закона Гесса.
Решение:
Теплоты образования DfН°298 жидкой и газообразной воды [Равдель]:
| Вещество | H2O(ж.) | H2O(г.) |
DfН°298, 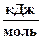
| –285,83 | –241,81 |
По 1-му следствию из закона Гесса (2.21):
DvН°298 = DfН°298(H2O(г.)) –DfН°298(H2O(ж.)) = –241,81 – (–285,83) = 44,02  .
.
Таким образом, испарение воды – это эндотермический процесс, т. е. протекает с поглощением теплоты.
Ответ: DvН°298 = 44,02  .
.
Второе следствие: тепловой эффект реакции DrН°T равен разности между суммами теплот сгорания исходных веществ и продуктов реакции, взятых с коэффициентами, равными стехиометрическим.
Этим следствием чаще всего пользуются при вычислении тепловых эффектов реакций с участием органических веществ, т. к. их теплоты сгорания легко определяются из опыта. Для реакции (2.19):
| DrН°T= [aDcН°T(A) + bDcН°T(B)] – [cDcН°T(C) + dDcН°T(D)] | (2.22) |
или в общем случае:
 . .
| (2.23) |
Пример 2.6. Рассчитайте тепловой эффект DrН°298 реакции этерификации щавелевой кислоты метиловым спиртом по 2-му следствию из закона Гесса.
(COOH)2(кр.) + 2CH3OH(ж.) ® (COOCH3)2(ж.) + 2H2O(ж.).
Решение:
Теплоты сгорания DcН°298 веществ – участников реакции [Равдель]:
| Вещество | (COOH)2(кр.) | CH3OH(ж.) | (COOCH3)2(ж.) | H2O(ж.) |
DcН°298, 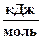
| –251,88 | –729,60 | –1680,2 |
По 2-му следствию из закона Гесса (2.22):
DrН°298 = [DcН°298((COOH)2(кр.)) + 2DcН°298(CH3OH(ж.))] – [DcН°298((COOCH3)2(ж.)) +
+ 2DcН°298(H2O(ж.))] = [–251,88 + 2×(–729,60)] – [–1680,2 + 2×0] = –30,88кДж.
Ответ: DrН°298 = –30,88 кДж.
При расчёте DrН°T по 2-му следствию из закона Гесса приходится сталкиваться с разностями больших чисел. Поэтому незначительные ошибки в теплотах сгорания могут привести к значительным ошибкам в вычисляемой величине DrН°T. Так ошибка в 1 % в DcН°298((COOCH3)2(ж.)) составляет 16,8 кДж, что для конечного результата DrН°298 составит 54,4 %.
Непосредственное определение теплот образования для многих веществ бывает затруднительно и даже невозможно. Например, теплоты образования органических веществ в большинстве случаев вычисляют на основании данных теплот сгорания соответствующих соединений.
Пример 2.7. Рассчитайте теплоту образования DfН°298 жидкого этилового спирта по 2-му следствию из закона Гесса.
Решение:
Реакция образования 1 моль жидкого этилового спирта из простых веществ:
2C(графит) + 3H2(г.) + 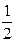 O2(г.) ® C2H5OH(ж.).
O2(г.) ® C2H5OH(ж.).
Теплоты сгорания DcН°298 веществ – участников реакции [Равдель]:
| Вещество | С(графит) | H2(г.) | O2(г.) | C2H5OH(ж.) |
DcН°298, 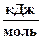
| –393,51 | –285,83 | –1370,68 |
По 2-му следствию из закона Гесса (2.23):
DfН°298(C2H5OH(ж.)) = DrН°298 =
[2DcН°298(C(графит)) + 3DcН°298(H2(г.)) +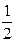 DcН°298(O2(г.))] –
DcН°298(O2(г.))] –
– DcН°298(C2H5OH(ж.)) = [2×(–393,51) + 3×(–285,83) + 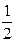 ×0] – (–1370,68) = –273,84
×0] – (–1370,68) = –273,84 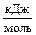 .
.
Отклонение рассчитанного значения DfН°298(C2H5OH(ж.)) от справочного (–276,98  ; [Равдель]) составляет 1,13 %.
; [Равдель]) составляет 1,13 %.
Ответ: DfН°298(C2H5OH(ж.)) = –273,84  .
.
Все рассмотренные в § 2.3 термохимические зависимости относятся к изобарным процессам (т. е. когда QP = DrH), т. к. большинство химических реакций протекают в открытых системах – при постоянных Р и Т. Однако, закон Гесса применим и для изохорных процессов (когда QV = DrU). Соотношение между DH и DU рассмотрено в § 2.2.
Дата добавления: 2016-06-29; просмотров: 4321;










