Самопроизвольные процессы. Энергия Гиббса
Процессы, протекающие без подвода энергии от внешнего источника, называются самопроизвольными. Например, образование ржавчины, реакция натрия с водой, растворение соли в воде и др.
Выясним критерии самопроизвольных процессов.
1. Большинство экзотермических реакций ( 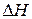 <0) протекают самопроизвольно. Однако существуют и эндотермические процессы, которые протекают самопроизвольно (растворение солей KCl и NH4NO3 в воде), следовательно,
<0) протекают самопроизвольно. Однако существуют и эндотермические процессы, которые протекают самопроизвольно (растворение солей KCl и NH4NO3 в воде), следовательно, 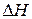 <0 - не критерий самопроизвольного процесса.
<0 - не критерий самопроизвольного процесса.
2. Кроме уменьшения 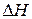 имеется другая движущая сила самопроизвольного процесса - это стремление частиц (молекул, ионов, атомов) к беспорядочному движению.
имеется другая движущая сила самопроизвольного процесса - это стремление частиц (молекул, ионов, атомов) к беспорядочному движению.
Энтропийный и энтальпийный факторы, взятые по отдельности, не могут быть критериями самопроизвольного течения химических реакций.
Для изобарно – изотермических процессов их объединяет функция, называемая энергией Гиббса:
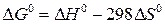 , (1)
, (1)
а в общем случае
 , (2)
, (2)
Эти уравнения позволяют вычислить  любой химической реакции, если известны
любой химической реакции, если известны 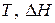 и
и 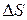 .
.
Стандартные энергии Гиббса 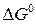 , энтальпии образования
, энтальпии образования  и энтропии
и энтропии 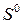 приводятся в справочных таблицах, в которых
приводятся в справочных таблицах, в которых 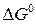 и
и  элементарных веществ в стандартном состоянии условно принимаются равными нулю.
элементарных веществ в стандартном состоянии условно принимаются равными нулю.
Как уже было упомянуто, движущая сила химической реакции определяется ее энергией Гиббса  .
. 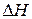 представляет энтальпийный, а
представляет энтальпийный, а 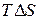 - энтропийный фактор. Первый из них отражает тенденцию системы к образованию связей в результате взаимного притяжения частиц – молекул или атомов, что приводит к их усложнению, а второй – тенденцию к усилению процессов диссоциации сложных частиц на более простые и их менее упорядоченному состоянию. Оба фактора обычно действуют в противоположных направлениях, и общее направление реакции определяется влиянием преобладающего фактора.
- энтропийный фактор. Первый из них отражает тенденцию системы к образованию связей в результате взаимного притяжения частиц – молекул или атомов, что приводит к их усложнению, а второй – тенденцию к усилению процессов диссоциации сложных частиц на более простые и их менее упорядоченному состоянию. Оба фактора обычно действуют в противоположных направлениях, и общее направление реакции определяется влиянием преобладающего фактора.
Энергия Гиббса служит критерием самопроизвольного протекания химической реакции при изобарно – изотермических процессах.
Химическая реакция принципиально возможна, если энергия Гиббса уменьшается, т.е.  <0. Чем больше отрицательное значение энергии Гиббса, тем полнее идет процесс. Уменьшение энергии Гиббса является условием возможности самопроизвольного течения реакции в прямом направлении.
<0. Чем больше отрицательное значение энергии Гиббса, тем полнее идет процесс. Уменьшение энергии Гиббса является условием возможности самопроизвольного течения реакции в прямом направлении.
Химическая реакция не может протекать самопроизвольно, если энергия Гиббса системы возрастает, т.е.  >0. Увеличение энергии Гиббса является условием невозможности самопроизвольного течения реакции в прямом направлении, а также служит термодинамическим условием возможности самопроизвольного протекания обратной реакции.
>0. Увеличение энергии Гиббса является условием невозможности самопроизвольного течения реакции в прямом направлении, а также служит термодинамическим условием возможности самопроизвольного протекания обратной реакции.
Наконец, если  =0, то реакция может протекать как в прямом, так и в обратном направлениях, т.е. реакция обратима.
=0, то реакция может протекать как в прямом, так и в обратном направлениях, т.е. реакция обратима.
Поскольку энергию Гиббса можно превратить в работу, то её также называют свободной энергией.
Если T → 0, то ΔG →ΔH. Таким образом, при низких температурах величина и знак ΔG определяются величиной и знаком ΔH. При низких температурах самопроизвольно протекают, как правило, экзотермические реакции.
Если T → ¥, то ΔG → TΔS. При высоких температурах величина и знак ΔG определяются величиной и знаком ΔS. При высоких температурах самопроизвольно протекают, как правило, реакции, ведущие к увеличению энтропии.
Таким образом, процессы в закрытой системе идут самопроизвольно в сторону понижения энергии Гиббса (ΔG = 0), что дает возможность установить границу, позволяющую судить о начале развития реакции в нужном направлении.
Для этого в уравнении: 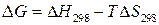 полагаем,
полагаем,  следовательно,
следовательно,  и
и 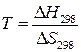 – температура при которой
– температура при которой  .
.
Изменение энергии Гиббса системы при образовании 1 моль вещества из простых веществ, устойчивых при 298 К, называется энергией Гиббса образования вещества.Если исходные вещества и продукты реакции находятся в стандартных состояниях, то энергия Гиббса называется стандартной энергией Гиббса химической реакции ΔG0 и является критерием самопроизвольного протекания реакции.
Используя закон Гесса, энергию Гиббса можно рассчитать как сумму энергий Гиббса образования продуктов реакции за вычетом энергий Гиббса образования исходных веществ с учетом стехиометрических коэффициентов:
ΔG = ∑nkΔGобр - ∑nнΔGобр.
Дата добавления: 2020-03-21; просмотров: 467;










