СТРОЕНИЕ ТВЕРДОГО ТЕЛА
Влияние типа связи на свойства кристалла
Типы твердых тел отличаются между собой по характеру сил взаимодействий, типу связи и тому, какие частицы расположены в узлах кристаллической решетки.
1. Кристаллы, в узлах которых правильно чередуются положительные и отрицательные ионы, имеют ионную связь. Вещества с ионной связью очень прочные, твердые, хрупкие. Обычно это вещества типа NaCl, KF,…
2. Ковалентная связь наблюдается у веществ типа Cl2.
3. Для металлической связи характерно наличие большого количества электронов, которые движутся среди ионов, образуя «электронный газ».
Аморфное и кристаллическое состояние
Твердые тела в зависимости от скорости охлаждения при кристаллизации делят на аморфные и кристаллические.
Аморфный металл получается при скоростях охлаждения 106…107 °С/с и более. Атомы при этом не располагаются в правильном порядке, не образуют кристаллов. Аморфное твердое тело является изотропным, т.е. обладает одинаковыми свойствами во всех направлениях. Кроме того, ему присущи высокая твердость, хорошая коррозионная стойкость и др. свойства. Если такое тело нагреть до определенной температуры, которая приведет к значительному повышению тепловой активности атомов, то аморфное состояние его перейдет в кристаллическое. Можно получить и смешанную структуру: аморфная основа и образовавшиеся в ней кристаллы.
В кристаллических твердых телах (при меньших скоростях охлаждения) атомы расположены в геометрически правильном порядке, образуя кристаллы и создавая кристаллическую решетку или воображаемую пространственную сетку.
Атомно-кристаллическая структура может быть представлена изображением не ряда периодически повторяющихся объемов, а одной элементарной ячейкой.
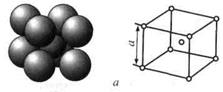
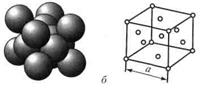
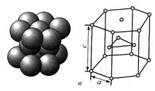
| Объемноцентрированный куб (ОЦК) | Гранецентрированный куб (ГЦК) | Гексагональная плотноупакованная (ГПУ) | ||
| 
| 
| ||
| а, с – параметры (периоды) решетки | ||||
| а=с | ||||
| К = 68 % | К = 74 % | К = 74 % | ||
| Na, K, V, Nb, Cr, Mo, W | Cu, Ag, Au, Pt, Al, Pb, Ni | Be, Mg, Zn, Cd | ||
Если принять, что атомы в решетке представляют собой упругие соприкасающиеся шары, то не трудно видеть, что в решетке помимо атомов, имеется значительное свободное пространство. Плотность кристаллической решетки, т.е. объем, занятый атомами, характеризуется коэффициентом компактности К. Расчеты компактности показали, что решетки ГЦК и ГП более компактны, чем ОЦК.
Некоторые металлы при разных температурах могут иметь различную кристаллическую решетку. Способность металла существовать в различных кристаллических формах носит название полиморфизма или аллотропии. При полиморфном превращении меняются форма и тип кристаллической решетки.
a – полиморфная модификация, устойчивая при более низких температурах;
g – полиморфная модификация, устойчивая при более высоких температурах.
Кристаллическим веществам свойственна анизотропия свойств, они имеют различные свойства в разных направлениях.
Дата добавления: 2020-02-05; просмотров: 161;










