Строение твердых веществ
В зависимости от расстояния между частицами и от сил взаимодействия между ними вещество может находиться в твердом, жидком и газообразном состояниях. При изменении давления и температуры одно состояние может переходить в другое. Твердое и жидкое состояние часто называют конденсированным.
Твердое вещество может находиться в аморфном и кристаллическом состоянии. Аморфное состояниеявляется метастабильным (с течением времени превращается в кристаллическое с выделением энергии), характеризуется изотропностью (одинаковостью значений свойств в любом направлении внутри вещества) и неупорядоченностью расположения частиц. Аморфные тела при нагреве размягчаются в большом температурном интервале, становятся вязкими, а затем переходят в жидкое состояние. Так, температурный интервал плавления силикатных стекол составляет 200°.

Кристаллические же тела остаются твердыми до определенной температуры, при которой они переходят в жидкое состояние

Они характеризуются упорядоченным расположением в пространстве частиц, образующих кристаллическую решетку. В кристалле частицы сближены до соприкосновения

Для упрощения пространственное изображение заменяют схемами, отмечая точками центры тяжести частиц

Если в кристалле провести три направления x, y, z, не лежащие в одной плоскости, то расстояния между частицами, расположенными по этим направлениям, в общем случае не одинаковы и соответственно равны a, b, c. Плоскости, параллельные координатным плоскостям, разбивают кристалл на множество таких одинаковых параллепипедов.

Наименьший параллепипед называют элементарной ячейкой. Для описания элементарной ячейки кристаллической решетки используют шесть величин: три отрезка, равные расстояниям a, b, c до ближайших частиц по осям координат, и три угла α, β, γ между этими отрезками. Соотношения между этими величинами определяются симметрией, согласно которой все кристаллы подразделяются на семь систем: триклинная, моноклинная, ромбическая, ромбоэдрическая, гексагональная, тетрагональная и кубическая. В большинстве случаев решетки имеют сложное строение, так как частицы находятся не только в узлах, но и на гранях или в центре решетки.
К основным характеристикам элементарной ячейки относятся:
1. Число частиц, приходящихся на одну элементарную ячейку (n)
2. Кратчайшее расстояние между частицами, образующими данный тип элементарной ячейки (l)
3. Координационное число,− число одинаковых частиц, расположенных на кратчайшем расстоянии от данной частицы (K)
4. Коэффициент компактности,− отношение объема всех частиц, приходящихся на одну элементарную ячейку, ко всему объему элементарной ячейки.
Все характеристики кубической элементарной ячейки связаны друг с другом соотношениями:



Рассмотрим следующие элементарные ячейки
| Примитивный куб ПК | Объемно-центрированный куб ОЦК | Гране-центрированный куб ГЦК | Алмазоподобная |
 n =
n =  l = a (ребро куба)
K = 6
l = a (ребро куба)
K = 6
|  n =
n =  l =
l =  a (половина диагонали куба)
K = 8 a (половина диагонали куба)
K = 8
|  n =
n =  l =
l =  a (половина диагонали грани куба)
K = 12 a (половина диагонали грани куба)
K = 12
|  n =
n =  l =
l =  a
K = 4 a
K = 4
|
Для ионных кристаллов элементарная ячейка характеризуется еще и числом формульных единиц (молекул) z
z = n/2, n = n(Kat+)+ n(An−)
l = r(Kat+)+ r(An−)

| Тип CsCl | Тип NaCl | Тип ZnS (сфалерит) |
 n(Cs+) =
n(Cs+) =  n(Cl−) = 1
n = n(Cl−) + n(Cs+) = 2
z =
n(Cl−) = 1
n = n(Cl−) + n(Cs+) = 2
z =  l =
l =  a
K = 8 a
K = 8
|  n(Cl−) =
n(Cl−) =  n(Na+) =
n(Na+) =  n = n(Cl−) + n(Na+) = 8
z =
n = n(Cl−) + n(Na+) = 8
z =  l =
l =  K = 6
K = 6
| 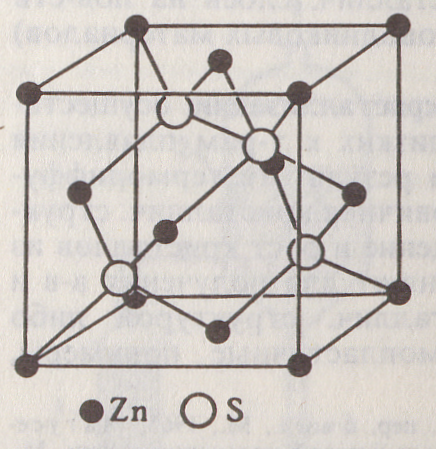 n(S2−) = 4
n(Zn2+) =
n(S2−) = 4
n(Zn2+) =  n = n(S2−) + n(Zn2+) = 8
z =
n = n(S2−) + n(Zn2+) = 8
z =  l =
l =  a
K = 4 a
K = 4
|
В зависимости от частиц, образующих кристалл, и характера связи между ними различают четыре типа кристаллических решеток:
1. Атомные – в узлах кристаллической решетки находятся нейтральные атомы, соединенные прочными ковалентными связями. Вещества с атомной кристаллической решеткой (алмаз, карбид кремния, кварц) химически инертны. Имеют высокие температуры кипения и плавления, высокую твердость.
2. Молекулярные – в узлах кристаллической решетки находятся молекулы, связанные слабыми водородными связями или межмолекулярными силами. Вещества с молекулярной кристаллической решеткой (кристаллы льда, кислорода, азота, галогенов, СО2, фенол, CrO3, Mn2O7) имеют низкую механическую прочность, низкие температуры плавления и кипения, а следовательно, высокую летучесть. Обычно такие вещества растворимы в неполярных растворителях, а в расплаве плохо проводят электрический ток.
3. Ионные – в узлах кристаллической решетки находятся положительно и отрицательно заряженные ионы, между которыми действуют электростатические силы притяжения. Энергия связи ионного кристалла по своему значению близка к энергии связи атомного кристалла. В связи с этим вещества (NaCl, NaNO3, Na3AlF6 и др. соли), имеющие ионную кристаллическую решетку, имеют высокие температуры кипения и плавления, обладают низкой летучестью и высокой твердостью.
4. Металлические – в узлах кристаллической решетки находятся атомы и катионы металлов, между которыми находятся валентные электроны. Такое строение решетки обусловливает у веществ (металлы) большую электро- и теплопроводность, высокую пластичность, блекс.
Среди кристаллов распространено явление полиморфизма – способность в твердом состоянии при различных температурах или давлении иметь различные типы кристаллических структур. Эти кристаллические структуры называются полиморфными модификациями. Например, для SiO2 известны три модификации: кварц, тридимит, кристобалит.
Полиморфизм элементов (аллотропия) – способность химических элементов существовать в виде двух и более простых веществ, различающихся по строению и свойствам. Например, С: графит, алмаз, карбин, фуллерен.
Способность различных веществ существовать в одной и той же кристаллической форме (например, KMnO4 и BaSO4 имеют одинаковую кристаллическую решетку), называется изоморфизмом.
Дата добавления: 2021-10-28; просмотров: 119;










